题目内容
3.运用元素周期律分析下列推断,其中错误的是( )| A. | 铍是一种轻金属,它的氧化物的水化物可能具有两性 | |
| B. | 砹单质是一种有色固体,砹化氢很不稳定 | |
| C. | 硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 | |
| D. | 硫酸锶难溶于水 |
分析 A.处于对角线上的元素性质具有相似性;
B.第VIIA族元素中,单质的颜色随着原子序数的增大而加深,氢化物的稳定性随着原子序数的增大而减弱;
C.元素的非金属性越弱,其氢化物越不稳定;
D.根据第IIA族元素碳酸盐溶解性的递变性判断.
解答 解:A.Be和Al处于对角线,其性质具有相似性,氢氧化铝具有两性,则氢氧化铍可能具有两性,故A正确;
B.第VIIA族元素中,单质的颜色随着原子序数的增大而加深,氢化物的稳定性随着原子序数的增大而减弱,所以砹单质是一种有色固体,砹化氢很不稳定,故B正确;
C.元素的非金属性越弱,其氢化物越不稳定,Se的非金属性小于S,则硒化氢(H2Se)不如H2S稳定,故C错误;
D.硫酸钙微溶于水、硫酸钡难溶于水,则硫酸锶难溶于水,故D正确;
故选C.
点评 本题考查了元素周期律的运用,明确元素周期律内涵是解本题关键,根据同一主族元素的递变性和相似性来分析解答,题目难度不大.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
13.化学实验在学科中有举足轻重的作用,结合下列实验的图示分析相关的描述正确的是( )
| A. | 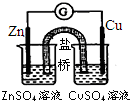 根据用电器(G)中指针的偏转方向可比较Zn、Cu的金属的氧化性 | |
| B. | 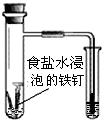 根据右侧小试管中液面的变化,可以判断铁钉发生了析氢腐蚀 | |
| C. | 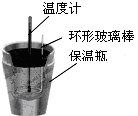 测定中和热 | |
| D. | 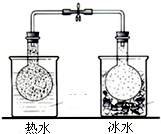 根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断2NO2(g)?N2O4(g)是一个放热反应 |
14.磷在自然界常以难溶于水的磷酸盐如Ca3(PO4)2等形式存在.它的单质和化合物有着广泛的应用.
(1)2P(s)+3Cl2(g)═2PCl3(g)△H=-612kJ/mol
P(s)+5/2Cl2(g)═PCl5(g)△H=-399kJ/mol
写出PCl5分解成PCl3和Cl2的热化学方程式是PCl5(g)═PCl3(g)+Cl2(g)△H=+93kJ•mol-1.
(2)PCl5分解成PCl3和Cl2的反应是可逆反应.T℃时,向2.0L恒容密闭容器中充入1.0mol PCl5,经过250s达到平衡.反应过程中测定的部分数据见下表:
反应在50~150s 内的平均速率v(PCl3)=1.5×10-4mol/(L•s).
(1)2P(s)+3Cl2(g)═2PCl3(g)△H=-612kJ/mol
P(s)+5/2Cl2(g)═PCl5(g)△H=-399kJ/mol
写出PCl5分解成PCl3和Cl2的热化学方程式是PCl5(g)═PCl3(g)+Cl2(g)△H=+93kJ•mol-1.
(2)PCl5分解成PCl3和Cl2的反应是可逆反应.T℃时,向2.0L恒容密闭容器中充入1.0mol PCl5,经过250s达到平衡.反应过程中测定的部分数据见下表:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
11.现代化学测定有机物组成及结构的分析方法较多.下列有关说法正确的是( )
| A. | 元素分析仪不仅可以测出试样常见的组成元素及含量,还可以测定其分子的空间结构 | |
| B. | 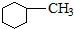 的核磁共振氢谱中有四组峰值1:2:2:3 的核磁共振氢谱中有四组峰值1:2:2:3 | |
| C. | 通过红外线光谱图分析可以区分乙醇和乙酸乙酯 | |
| D. | 质谱法和紫外光谱法不属于测定有机物组成和结构的现代分析方法 |
15.下列事实不能用电化学原理解释的是( )
| A. | 铁片在潮湿的环境中生锈 | |
| B. | 远洋海轮的尾部装上一定数量的锌板 | |
| C. | 银制器皿露置在空气中发黑 | |
| D. | 用锌与硫酸制氢气时,往硫酸中滴少量硫酸铜 |
13.下列叙述中正确的是( )
| A. | 相同条件下,N2和O3的混合气体与等体积的N2所含原子数相等 | |
| B. | 标准状况下,28 g CO和22.4 L SO3所含分子数相等 | |
| C. | 5.6 g铁粉与足量氯气充分反应,有0.2 mol电子转移 | |
| D. | 等物质的量的CH${\;}_{5}^{+}$和NH${\;}_{2}^{-}$所含电子数相等 |

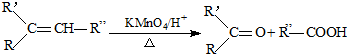
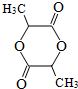 .
.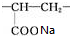 .
.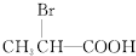 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$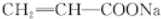 +NaBr+2H2O
+NaBr+2H2O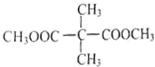 .
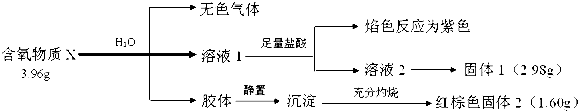
. 
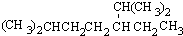
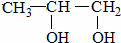 <
< 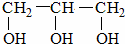 (填“>”“<”或“=”,下同)
(填“>”“<”或“=”,下同) <
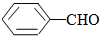
<
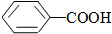 >CH3COOH(提示:类比酚与醇的酸性)
>CH3COOH(提示:类比酚与醇的酸性)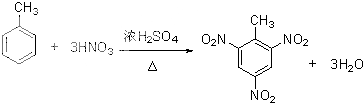 ;
;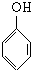 +nHCHO
+nHCHO 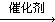
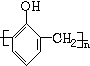 +nH2O.
+nH2O.