题目内容
13.下列叙述中正确的是( )| A. | 相同条件下,N2和O3的混合气体与等体积的N2所含原子数相等 | |
| B. | 标准状况下,28 g CO和22.4 L SO3所含分子数相等 | |
| C. | 5.6 g铁粉与足量氯气充分反应,有0.2 mol电子转移 | |
| D. | 等物质的量的CH${\;}_{5}^{+}$和NH${\;}_{2}^{-}$所含电子数相等 |
分析 A.从N2和O3的分子组成分析,1molN2含有2mol原子,1molO3含有3mol原子;
B.气体摩尔体积只适用于气体,标准状况三氧化硫不是气体;
C.氯气具有强氧化性,变价金属生成高价,铁和氯气反应会生成氯化铁;
D.CH5+和NH2-所含电子数分别是10、10;
解答 解:A.相同条件下,N2和O3的混合气体与等体积的N2的物质的量相同,则分子数相同,但N2和O3的分子组成原子数目不同,则所含原子数不等,故A错误;
B.标准状况下,28g CO的物质的量为$\frac{28g}{28g/mol}$=1mol,气体摩尔体积只适用于气体,标况下,三氧化硫不是气体,不能使用气体摩尔体积,SO3物质的量不是1mol,故B错误;
C.5.6g即0.1mol铁粉与足量氯气充分反应,生成氯化铁,有0.3mol电子转移,故C错误;
D.等物质的量的CH5+和NH2+所含电子的物质的量分别是10mol和10mol,数目相等,故D正确;
故选D.
点评 本题涉及物质的量的有关计算知识,注意知识的迁移和应用,注意阿伏加德罗定律及推论的应用,题目难度中等,注意把握粒子的组成原子的结构特点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.运用元素周期律分析下列推断,其中错误的是( )
| A. | 铍是一种轻金属,它的氧化物的水化物可能具有两性 | |
| B. | 砹单质是一种有色固体,砹化氢很不稳定 | |
| C. | 硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 | |
| D. | 硫酸锶难溶于水 |
4.下列对反应2H2SO4+Cu→CuSO4+SO2↑+2H2O的说法中正确的是( )
| A. | 氧化剂与还原剂的物质的量之比为2:1 | |
| B. | 氧化产物与还原产物的物质的量之比为1:1 | |
| C. | 该反应说明Cu的金属性很强 | |
| D. | 2mol H2SO4参与反应时,有4 mol电子发生转移 |
1.下列叙述错误的是( )
| A. | 苯、乙烯都既能发生加成反应,也能发生氧化反应 | |
| B. | 塑料、橡胶和合成纤维都属于有机高分子化合物 | |
| C. | 淀粉、葡萄糖、脂肪和蛋白质在一定条件下都能发生水解反应 | |
| D. | 淀粉、纤维素的通式均为(C6H10O5)n,但它们不互为同分异构体 |
8.下列物质中不能使品红溶液褪色的是( )
| A. | 过氧化钠 | B. | 二氧化硫 | C. | 盐酸 | D. | 氯气 |
5.下列有关化学用语的说法中正确的是( )
| A. | -OH与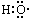 都表示羟基 都表示羟基 | B. | 聚丙烯的结构简式: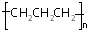 | ||
| C. | CH4分子的比例模型: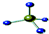 | D. | 次氯酸分子的电子式: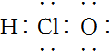 |
2.下列气态氢化物按稳定性由强到弱顺序的是( )
| A. | HBr、HCl、HF | B. | HF、H2O、NH3 | C. | NH3、PH3、H2S | D. | SiH4、CH4、NH3 |
16.在电冶铝的电解槽中存在电解质W3XZ6-XZ3-X2Y3,己知X、Y、Z、W四种元素的简单离子的电子层结构均相同.X原子最外层电子数等于电子层数,则下列说法正确的是( )
| A. | 原予序数:W>X>Y>Z | |
| B. | 原子半径:r(W)>r(X)>r(Y)>r(Z) | |
| C. | 最高价氧化物对应的水化物碱性:w<x | |
| D. | 在电解过程中,W3XZ6的主要作用是增强电解质的导电性 |
 利用如图所示装置收集以下8种气体(图中烧瓶的位置不得变化):
利用如图所示装置收集以下8种气体(图中烧瓶的位置不得变化):