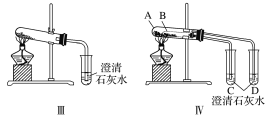
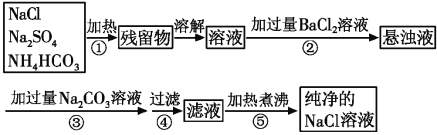
题目内容
【题目】有机物Z是制备药物的中间体,合成Z的路线如下图所示,下列有关叙述不正确的是

A. X的分子式为C8H8O2
B. X、Y、Z均能和NaOH溶液反应
C. 可用NaHCO3溶液鉴别Y和Z
D. 1mol X跟足量H2反应,最多消耗4mol H2
【答案】D
【解析】
A. 根据X的结构式,X的分子式为C8H8O2,故A正确;
B. X含有酯基,Y含有酚羟基,Z含有羧基均能和NaOH溶液反应,故B正确;
C. Y中含有酚羟基,结合苯酚的性质,可电离出氢离子,不能使酸性指示剂变色,其酸性比碳酸还弱,不与NaHCO3溶液反应; Z为有机酸,酸性比碳酸强,与NaHCO3溶液反应释放出二氧化碳气体;故C正确;
D. X中酯基上的碳氧双键不发生加成反应,1mol X跟足量H2反应,最多消耗3mol H2,故D错误;
答案选D。

【题目】雾霾天气严重影响人们的生活,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一,以下方法可以消除氮氧化物和硫氧化物的污染。
(1)用活性炭还原法可处理氮氧化物,向某密闭容器中加入一定量的活性炭和NO,发生反应:![]() △H<0,在一定条件下,反应进行到不同时间测得各物质的浓度如下表。
△H<0,在一定条件下,反应进行到不同时间测得各物质的浓度如下表。
时间/min 浓度/mol·L-1 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.52 | 0.40 | 0.40 | 0.44 | 0.44 |
N2 | 0 | 0.24 | 0.30 | 0.30 | 0.28 | 0.28 |
CO2 | 0 | 0.24 | 0.30 | 0.30 | 0.28 | 0.28 |
①0~10min内,NO的平均反应速率v(NO)=_______________。
②在恒容条件下,能判断该反应一定达到化学平衡状态的标志是_________(填字母编号)。
a.v正(N2)=2v逆(NO) b.反应体系的压强不再发生改变
c.![]() 不变 d.混合气体的密度保持不变
不变 d.混合气体的密度保持不变
③30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是___________。
(2)NH3催化还原氮氧化物技术是目前应用最广泛的烟气氮氧化物脱除技术。已知c(NO2):c(NO)=1:1时脱氮效果最佳,若生成1mol N2时反应放出的热量为Q kJ。此时对应的脱氮反应的热化学方程式为_____________________________________________________。
(3)利用钠碱循环法可脱除烟气中的SO2。
①在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是_____________________。
②吸收液吸收SO2的过程中,pH随n(![]() ):n(
):n(![]() )变化关系如下表:
)变化关系如下表:
n( | 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:

写出![]() 在阳极放电的电极反应式:_______________________________________,当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。
在阳极放电的电极反应式:_______________________________________,当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。
(4)利用喷雾干燥法脱硫工艺是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收。该温度下吸收液中c(Ca2+)一直保持为0.50 mol·L-1,已知KSP(CaSO3)=1.4×10-7,求吸收后溶液中![]() 的浓度______________________。
的浓度______________________。