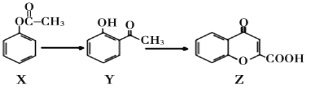
��Ŀ����
����Ŀ��ijУ��ѧ����С��Ϊ�˼���̼���ƺ�̼���������ְ�ɫ���壬�ò�ͬ�ķ�����������ʵ�飬��ͼ����ʾ��
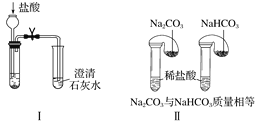
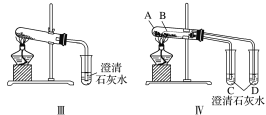
��1��ͼ����ʾʵ���У�__(�����)�ܹ��Ϻôﵽʵ��Ŀ�ġ�
��2��ͼ����ʾʵ����ܼ������������ʣ�����ʵ��ķ���װ���з�Ӧ�Ļ�ѧ����ʽΪ��__����ʵ�����ȣ�ʵ������ŵ���___(����ĸ)��
A.���Ȣ���
B.���Ȣ�ȫ
C.���Ȣ�������
D.������������һ��װ��ͬʱ���������Ա�ʵ�飬������
��3������ʵ�����֤̼���ƺ�̼�����Ƶ��ȶ��ԣ����Թ�B��װ��Ĺ��������__(�ѧʽ)��
���𰸡��� 2NaHCO3![]() Na2CO3��H2O��CO2�� D NaHCO3
Na2CO3��H2O��CO2�� D NaHCO3
��������
(1) ͼ���ʾ���ʺ����ᷴӦ���ɶ�����̼�����߶����Բ��������𣬢���ʵ��Ϊ���߶������ᷴӦ�����Dz�������Ŀ��������������ͬ����������̼���ƺ�̼�����ƣ�����ʵ����ܴﵽ�Ϻõ�ʵ��Ŀ�ģ�
(2)̼�����������ȷֽ�����̼���ƺ�ˮ�Ͷ�����̼������ʽΪ�� 2NaHCO3![]() Na2CO3+H2O+CO2������ʵ�����ȣ�ʵ������ŵ���һ�����������ʵ�ʵ�飬�Ա��������ԣ���ѡD��
Na2CO3+H2O+CO2������ʵ�����ȣ�ʵ������ŵ���һ�����������ʵ�ʵ�飬�Ա��������ԣ���ѡD��
(3)Ϊ�˸�����֤̼�����ƵIJ��ȶ��ԣ������С�Թ��м���̼�����ơ�

����Ŀ��Li4Ti5O12��LiFePO4��������ӵ�صĵ缫���ϣ���������������Ҫ�ɷ�ΪFeTiO3������������MgO��SiO2�����ʣ����Ʊ��������������£�
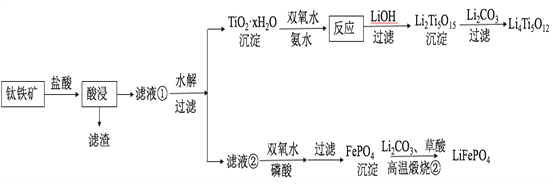
�ش��������⣺
��1���������ʵ���У����Ľ����ʽ������ͼ��ʾ����ͼ��֪�������ľ�����Ϊ70%ʱ�������õ�ʵ������Ϊ___________________��
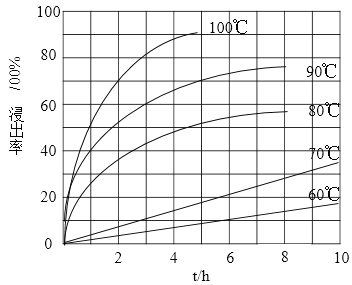
��2���������������Ҫ��TiOCl42����ʽ���ڣ�д����Ӧ��Ӧ�����ӷ���ʽ__________________��
��3��TiO2��xH2O������˫��ˮ����ˮ��Ӧ40 min����ʵ�������±���ʾ��
�¶�/�� | 30 | 35 | 40 | 45 | 50 |
TiO2��xH2Oת����% | 92 | 95 | 97 | 93 | 88 |
����40��ʱTiO2��xH2Oת������ߵ�ԭ��__________________��
��4��Li2Ti5O15��Ti�Ļ��ϼ�Ϊ+4�����й���������ĿΪ__________________��
��5��������Һ�ڡ���c(Mg2+)=0.02 mol/L������˫��ˮ�����ᣨ����Һ�������1������ʹFe3+ǡ�ó�����ȫ����Һ��c(Fe3+)=1��10-5 mol/L����ʱ�Ƿ���Mg3(PO4)2�������ɣ�___________����ʽ���㣩��
FePO4��Mg3(PO4)2��Ksp�ֱ�Ϊ1.3��10-22��1.0��10-24��
��6��д�����������բڡ�����FePO4�Ʊ�LiFePO4�Ļ�ѧ����ʽ______��