题目内容
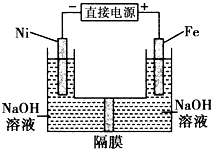 高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )
高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )| A、铁是阳极,电极反应为Fe-6e-+4H2O═FeO42-+8H+ |
| B、镍电极上的电极反应为2H2O+2e-═H2↑+2OH- |
| C、若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D、电解时阳极区pH降低、阴极区pH升高,最终溶液pH不变 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:铁是阳极,电极反应式为Fe-6e-+8OH-═FeO42-+4H2O,Ni电极上氢离子放电,电极反应式为2H2O+2e-═H2↑+2OH-,据此分析解答.
解答:
解:A.铁是阳极,电极反应为Fe-6e-+8OH-═FeO42-+4H2O,碱性条件下不能生成氢离子,故A错误;
B.镍电极上氢离子放电生成氢气,电极反应式为2H2O+2e-═H2↑+2OH-,故B正确;
C.Ni电极附近生成氢氧根离子,阳极上氢氧根离子参加反应,所以OH-自左向右移动,故C错误;
D.电解时阳极区pH降低、阴极区pH升高,当转移电子相等时,发生反应Fe+2H2O+2OH-═FeO42-+3H2↑,则混合溶液中氢氧根离子浓度减小,溶液的pH降低,故D错误;
故选B.
B.镍电极上氢离子放电生成氢气,电极反应式为2H2O+2e-═H2↑+2OH-,故B正确;
C.Ni电极附近生成氢氧根离子,阳极上氢氧根离子参加反应,所以OH-自左向右移动,故C错误;
D.电解时阳极区pH降低、阴极区pH升高,当转移电子相等时,发生反应Fe+2H2O+2OH-═FeO42-+3H2↑,则混合溶液中氢氧根离子浓度减小,溶液的pH降低,故D错误;
故选B.
点评:本题考查了电解池原理,明确各个电极上发生的反应是解本题关键,注意阳极发生的反应,易错选项是D,根据总方程式判断,为易错点.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
下列各组物质互为同系物的是( )
| A、金刚石和石墨 |
| B、正丁烷和异丁烷 |
| C、甲烷和乙烷 |
| D、白磷和红磷 |
化学与科技、社会、生产密切结合,下列有关说法正确的是( )
| A、“纯净水”清洁、纯净,长期饮用有益健康 |
| B、维生素C不宜与含硫酸亚铁的补血剂同服 |
| C、在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
| D、味觉上具有酸味的食物即酸性食物,长期食用会导致血液偏酸性,引起缺钙 |
下列原理或操作不正确的是( )
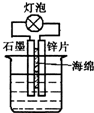

| A、在如图装置的稀硫酸中加入适量重铬酸钾或适量6%的H2O2溶液,可以使灯泡亮度增大,持续时间变长 |
| B、纸层析法分离微量成份时均需有以下流程:装置制作→点层析试样→配制展开剂→层析操作→显色反应 |
| C、在提纯混有少量NaCl的KNO3时,常先将混合物在较高温度下溶于水形成浓溶液,再经过冷却结晶、过滤、洗涤、干燥,获得KNO3晶体 |
| D、制摩尔盐时用酒精洗涤产品,用干净的滤纸吸干;而在制阿司匹林粗品时用冷水洗涤产品,在空气中风干 |
在由水电离出的c(H+)=1×10-13mol/L的溶液中,一定可以大量共存的是( )
| A、Ba2+Na+ NO3-Cl- |
| B、Fe2+ Na+ NO3- Cl- |
| C、SO42-SO32- NH4+Na+ |
| D、Mg2+Na+Br-AlO2- |
下列关于甲、乙、丙、丁四个图象的说法中,正确的是( )
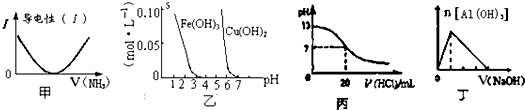

| A、图甲表示向乙酸溶液中通入NH3过程中溶液导电性的变化 |
| B、由图乙可知若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO至pH在4左右 |
| C、图丙表示25°C时,用0.1mol/L盐酸滴定20mL 0.1mol.L-1氨水,溶液的pH随加入盐酸体积的变化 |
| D、图丁表示向Al2(SO4)3溶液中滴入NaOH溶液,生成Al(OH)3沉淀的量随NaOH溶液体积的变化 |
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、46g有机物C2H6O中含有的H-O键的数目为NA |
| B、常温下,2L 1mol?L-1的乙酸溶液中,所含分子总数小于2NA |
| C、标准状况下,5.6L NO和5.6L O2组成的混合气体中所含原子数为NA |
| D、18g D2O含有的电子总数为10NA |