题目内容
下列有关电极和电解质溶液构成的装置叙述不正确的是( )
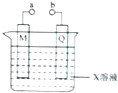

| A、若X、M、Q分别是H2SO4、Pb和PbO2,a、b连接后两极都有PbSO4生成 |
| B、若X、M、Q分别是CuSO4、Ag和Fe无论a、b是否连接Fe都被腐蚀 |
| C、若X、M、Q分别CuSO4、Cu和Fe,a、b是分别连接电源的正负极,则可对铁镀铜 |
| D、若X、M、Q分别是NaCl、C和Fe,则a、b连接后,M电极上有气体产生 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.若X、M、Q分别是H2SO4、Pb和PbO2,为铅蓄电池;
B.若X、M、Q分别是CuSO4、Ag和Fe,a、b相连时形成原电池,不相连时,铁可置换出银;
C.若X、M、Q分别CuSO4、Cu和Fe,a、b是分别连接电源的正负极,为电镀装置,铜为阳极;
D.若X、M、Q分别是NaCl、C和Fe,则a、b连接后,铁发生吸氧腐蚀.
B.若X、M、Q分别是CuSO4、Ag和Fe,a、b相连时形成原电池,不相连时,铁可置换出银;
C.若X、M、Q分别CuSO4、Cu和Fe,a、b是分别连接电源的正负极,为电镀装置,铜为阳极;
D.若X、M、Q分别是NaCl、C和Fe,则a、b连接后,铁发生吸氧腐蚀.
解答:
解:A.若X、M、Q分别是H2SO4、Pb和PbO2,为铅蓄电池,铅蓄电池放电时,正极上PbO2得电子被还原,电极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,负极上铅失电子发生氧化反应,电极反应式为 Pb(s)+SO42-(aq)-2e-=PbSO4(s),都生成PbSO4,故A正确;
B.若X、M、Q分别是CuSO4、Ag和Fe,a、b相连时形成原电池,铁为负极,被氧化,不相连时,铁可置换出银,故B正确;
C.若X、M、Q分别CuSO4、Cu和Fe,a、b是分别连接电源的正负极,为电镀装置,铜为阳极,可在铁上镀铜,故C正确;
D.若X、M、Q分别是NaCl、C和Fe,则a、b连接后,铁发生吸氧腐蚀,没有气体生成,故D错误.
故选D.
B.若X、M、Q分别是CuSO4、Ag和Fe,a、b相连时形成原电池,铁为负极,被氧化,不相连时,铁可置换出银,故B正确;
C.若X、M、Q分别CuSO4、Cu和Fe,a、b是分别连接电源的正负极,为电镀装置,铜为阳极,可在铁上镀铜,故C正确;
D.若X、M、Q分别是NaCl、C和Fe,则a、b连接后,铁发生吸氧腐蚀,没有气体生成,故D错误.
故选D.
点评:本题考查较为综合,涉及原电池、电解池的综合考查,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握原电池、电解池的工作原理以及电极方程式的书写,难度不大.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
下列数量的各物质所含原子个数由大到小顺序排列的是( )
①0.5mol氨气 ②4g氦气 ③4℃时9mL水 ④0.2mol磷酸钠.
①0.5mol氨气 ②4g氦气 ③4℃时9mL水 ④0.2mol磷酸钠.
| A、④③②① | B、①④③② |
| C、②③④① | D、①④②③ |
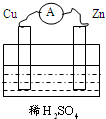 如图将Cu、Zn两种金属片插入稀H2SO4中,构成铜锌原电池,下列关于铜锌原电池的叙述正确的是( )
如图将Cu、Zn两种金属片插入稀H2SO4中,构成铜锌原电池,下列关于铜锌原电池的叙述正确的是( )| A、溶液中的H+向负极移动 |
| B、Zn片作负极,发生还原反应 |
| C、溶液的PH值将增大 |
| D、电子从Cu流出经导线流向Zn |
下列各组物质互为同系物的是( )
| A、金刚石和石墨 |
| B、正丁烷和异丁烷 |
| C、甲烷和乙烷 |
| D、白磷和红磷 |
下列有关电解质溶液的说法正确的是( )
| A、将pH=2的NH4Cl与pH=12氨水等体积混合,溶液中:c(NH4+)=c(Cl-) | ||||
| B、溶液中c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) | ||||
| C、1.0mol?L-1的H2SO4溶液80℃时的pH大于25℃时pH | ||||
D、对氨水进行稀释,
|
甲基环己烷可由甲苯与氢气加成制得,其环上一氯代物的同分异构体数目是( )
| A、4 | B、3 | C、2 | D、1 |
化学与科技、社会、生产密切结合,下列有关说法正确的是( )
| A、“纯净水”清洁、纯净,长期饮用有益健康 |
| B、维生素C不宜与含硫酸亚铁的补血剂同服 |
| C、在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
| D、味觉上具有酸味的食物即酸性食物,长期食用会导致血液偏酸性,引起缺钙 |
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、46g有机物C2H6O中含有的H-O键的数目为NA |
| B、常温下,2L 1mol?L-1的乙酸溶液中,所含分子总数小于2NA |
| C、标准状况下,5.6L NO和5.6L O2组成的混合气体中所含原子数为NA |
| D、18g D2O含有的电子总数为10NA |
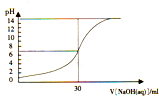 常温下,15ml某待测物质的量浓度的盐酸,用一定物质的量浓度的NaOH溶液滴定的滴定曲线如图所示,则两种溶液的物质量的浓度分别是( )
常温下,15ml某待测物质的量浓度的盐酸,用一定物质的量浓度的NaOH溶液滴定的滴定曲线如图所示,则两种溶液的物质量的浓度分别是( )