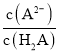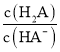题目内容
【题目】pH=12的NaOH和pH=4的HCl等体积混合的pH=_____________
【答案】11.7
【解析】
先计算酸溶液中c(H+)、根据水的离子积常数、溶液的pH,计算碱溶液中c(OH-),然后根据H+、OH-的物质的量关系判断哪种物质过量,再计算混合后溶液中c(H+),最后根据pH= -lg c(H+)计算。
pH=12的NaOH,c(OH-)=10-2mol/L,pH =4的HCl,c(H+)=10-4mol/L,则二者等体积混合时,溶液中碱过量,溶液显碱性,混合溶液中c(OH-)(碱)=![]() mol/L=5×10-3mol/L,根据水的离子积常数可知c(H+)=
mol/L=5×10-3mol/L,根据水的离子积常数可知c(H+)=![]() =2×10-12mol/L,所以溶液的pH= -lgc(H+)=12-0.3=11.7。
=2×10-12mol/L,所以溶液的pH= -lgc(H+)=12-0.3=11.7。

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目