题目内容
【题目】如图所示是制取SO2并验证SO2某些性质的装置图
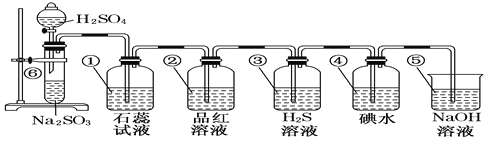
试回答:
(1)⑥中发生反应的化学方程式为______________________________________。
(2)①中的实验现象为________________________________________________。
(3)观察到②中的品红溶液________,证明SO2有________。
(4)观察到③中的H2S溶液________,证明SO2有_____________。
(5)观察到④中的碘水________,证明SO2有________。
(6)⑤中NaOH溶液的作用是_________,有关反应的化学方程式为:_________________,此反应说明SO2是________氧化物
【答案】 Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O 溶液变红 褪色 漂白性 出现浅黄色沉淀(或变浑浊) 氧化性 褪色 还原性 吸收多余的SO2,防止其污染环境 2NaOH+SO2===Na2SO3+H2O 酸性
【解析】本题主要考查SO2的实验室制备及性质实验。⑥中Na2SO3+H2SO4══Na2SO4+H2O+SO2↑,①中SO2气体通过石蕊试液,由于SO2溶于水生成H2SO3具有酸性,石蕊变红。② SO2通过品红溶液褪色,通过③发生SO2+H2S══3S↓+2H2O反应,通过④发生 SO2+I2+H2O══H2SO4+2HI;通过⑤反应为SO2+2NaOH══Na2SO3+H2O,吸收多余的SO2,防止空气污染。能与碱反应盐和水,说明SO2是一种酸性氧化物。

【题目】已知:反应I:4NH3(g)+6NO(g)5N2(g)+6H2O(l)△H1反应Ⅱ:2NO(g)+O2(g)2NO2(g)△H2(且|△H1|=2|△H2|)
反应Ⅲ:4NH3(g)+6NO2(g)5N2(g)+3O2(g)+6H2O(l)△H 3
反应I和反应Ⅱ在不同温度时的平衡常数及其大小关系如下表
温度/K | 反应I | 反应II | 已知: |
298 | K1 | K2 | |
398 | K1′ | K2′ |
(1)△H3=(用△H1、△H2的代数式表示);推测反应Ⅲ是反应(填“吸热”或“放热”)
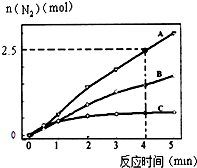
(2)相同条件下,反应I:4NH3(g)+6NO(g)5N2(g)+6H2O(l)在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示. ①计算0~4分钟在A催化剂作用下,反应速率V(NO)= .
②下列说法不正确的是 .
A.单位时间内H﹣O键与N﹣H键断裂的数目相等时,说明反应已经达到平衡
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
D.增大压强能使反应速率加快,是因为增加了活化分子百分数
(3)一定条件下,反应II达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2. ①保持恒温恒容,再充入NO2气体,NO2体积分数(填“变大”、“变小”或“不变”)
②关于平衡体系反应Ⅱ:2NO(g)+O2(g)2NO2(g);△H2说法正确的是 .
A、该反应焓变为负值
B、升高温度,逆反应速率增大,正反应速率减小,反应逆向移动
C、不论增大压强还是减小压强,正方向速率改变的程度更大
D、平衡正向移动,NO的转化率一定增大
E、平衡体系中加入NO2 , 平衡逆向移动,△H2减小
F、混合气体颜色加深说明平衡向右移动,颜色变浅则向左移动.