题目内容
【题目】已知:A(g)+2B(g)C(g)+D(g)△H<0,一定温度下,2molA和2molB在2L密闭容器中反应,10min后达到平衡,此时容器压强降为原来的 ![]() ,下列叙述正确的是( )
,下列叙述正确的是( )
A.从开始到平衡,A的反应速率为0.08mol?L﹣1?min﹣1
B.随着反应的进行,混合气体的密度逐渐减小
C.达到平衡时,B的转化率为20%
D.该温度下,反应的平衡常数K= ![]()
【答案】D
【解析】解:已知:A(g)+2B(g)C(g)+D(g)△H<0,一定温度下,2molA和2molB在2L密闭容器中反应,10min后达到平衡,结合化学三行计算得到,设A消耗物质的量为x,
A(g)+ | 2B(g) | C(g)+ | D(g) | |
起始量(mol) | 1 | 2 | 0 | 0 |
变化量(mol) | X | 2x | X | X |
平衡量(mol) | 2-x | 2-2x | x | X |
此时容器压强降为原来的 ![]() ,气体物质的量之比等于气体压强之比,
,气体物质的量之比等于气体压强之比,
2﹣x+2﹣2x+x+x= ![]() ×(2+2)
×(2+2)
x=0.8mol,
A.从开始到平衡,A的反应速率v= ![]() =
= ![]() =0.04molL﹣1min﹣1 , 故A错误;
=0.04molL﹣1min﹣1 , 故A错误;
B.反应前后气体体积不变,气体质量不变,密度ρ= ![]() ,随着反应的进行,混合气体的密度始终不变,故B错误;
,随着反应的进行,混合气体的密度始终不变,故B错误;
C.达到平衡时,B的转化率= ![]() ×100%=
×100%= ![]() ×100%=80%,故C错误;
×100%=80%,故C错误;
D.K= 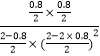 =
= ![]() ,故D正确;
,故D正确;
故选D.
【考点精析】利用化学平衡的计算对题目进行判断即可得到答案,需要熟知反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目