题目内容
电子层数相同的元素随着原子序数的递增,原子半径依次 ,核电荷数依次 ,核对最外层电子的引力依次 ,原子失去电子的能力逐渐 ,得电子的能力逐渐 ,所以金属性依次 ,非金属性依次 .
考点:同一周期内元素性质的递变规律与原子结构的关系,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:电子层数相同的元素,处于同周期,随着原子序数的递增,原子半径减小,核电荷数增大,核对最外层电子的引力增强,失电子能力减弱,得电子能力增强,则金属性减弱,非金属性增强,以此来解答.
解答:
解:电子层数相同的元素随着原子序数的递增,元素性质出现递变规律,原子半径依次减小,核电荷数依次增大,核对最外层电子的引力依次增强,原子失去电子的能力逐渐减弱,得电子的能力逐渐减弱,所以金属性依次减弱,非金属性依次增强,
故答案为:减小;增大;增强;减弱;增强;减弱;增强.
故答案为:减小;增大;增强;减弱;增强;减弱;增强.
点评:本题考查同周期元素的性质,为高频考点,把握同周期元素性质的变化规律为解答的关键,注重基础知识的考查,属于记忆性知识点,题目难度不大.

练习册系列答案
相关题目
在盐类发生水解的过程中正确的说法是( )
| A、盐的电离平衡被破坏 |
| B、水的电离度逐渐增大 |
| C、溶液的pH发生改变 |
| D、没有中和反应发生 |
某化学实验报告中有如下记录,其中实验数据合理的是( )
| A、用25mL酸式滴定管量取5.6mL的稀硝酸 |
| B、用广泛的pH试纸测得溶液的pH为6.2 |
| C、温度计显示的室温读数为25.69℃ |
| D、用托盘天平称取11.7g CuO粉末 |
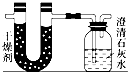 已知某醇燃料含有碳、氢、氧三种元素.为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如下表所列的实验结果(假设产生的气体完全被吸收):
已知某醇燃料含有碳、氢、氧三种元素.为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如下表所列的实验结果(假设产生的气体完全被吸收): 已知一定量的有机物A在氧气中完全燃烧,只生成0.2mol CO2和0.3mol H2O,试回答下列问题:
已知一定量的有机物A在氧气中完全燃烧,只生成0.2mol CO2和0.3mol H2O,试回答下列问题: