题目内容
在盐类发生水解的过程中正确的说法是( )
| A、盐的电离平衡被破坏 |
| B、水的电离度逐渐增大 |
| C、溶液的pH发生改变 |
| D、没有中和反应发生 |
考点:盐类水解的原理
专题:盐类的水解专题
分析:A、盐的水解是盐溶液中的弱离子和水电离出的氢离子或是氢氧根离子结合形成弱电解质的过程;
B、根据盐的水解实质和内涵来回答;
C、盐的水解会导致有的盐溶液显示酸碱性;
D、(H+)与c(OH-)的乘积受温度的影响.
B、根据盐的水解实质和内涵来回答;
C、盐的水解会导致有的盐溶液显示酸碱性;
D、(H+)与c(OH-)的乘积受温度的影响.
解答:
解:A、盐类水解的过程中,水的电离平衡被破坏,盐是能完全电离的,不存在平衡,故A错误;
B、盐类水解的过程是对水的电离平衡的促进过程,故B正确;
C、盐的水解会导致有的盐溶液显示酸碱性,水解平衡不移动,盐的酸碱性不变,故C错误;
D、盐类水解是酸碱中和反应的逆反应,存在水解平衡,有中和反应发生,故D错误.
故选B.
B、盐类水解的过程是对水的电离平衡的促进过程,故B正确;
C、盐的水解会导致有的盐溶液显示酸碱性,水解平衡不移动,盐的酸碱性不变,故C错误;
D、盐类水解是酸碱中和反应的逆反应,存在水解平衡,有中和反应发生,故D错误.
故选B.
点评:本题考查学生盐的水解原理以及盐的电离知识,注意知识的梳理和归纳是解题的关键,难度不大.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、在反应KIO3+6 HI=KI+3I2十3 H2O中,每生成3mo1 I2转移的电子数为5NA |
| B、100mL 18.4mo1?L-1硫酸与足量Cu反应,生成SO2的分子数为0.92NA |
| C、1 L 0.1 moI?L-1的CH3COOH溶液中所含的离子和分子总数为0.1NA |
| D、将0.lmol FeC13滴人沸水中可制得0.1NA Fe(OH)3胶粒 |
常温下,下列对醋酸稀溶液的叙述中,正确的是( )
A、将pH=a的醋酸稀释变为pH=a+1,醋酸的浓度则变为原来的
| ||
B、将pH=a的醋酸稀释为pH=a+1的过程中,
| ||
| C、pH=a的醋酸与pH=a+1的醋酸分别中和等物质的量的NaOH溶液,二者所消耗体积比为1:10 | ||
| D、等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,存在a+b=14 |
只能表示一个化学反应的离子方程式为( )
| A、BaCO3+2CH3COOH═Ba2++CO2↑+H2O+2CH3COO- |
| B、Ba2++2OH-+2H++SO42-═2H2O+BaSO4↓ |
| C、CH3COOH+OH-═CH3COO-+H2O |
| D、Fe3++3NH3?H2O═Fe(OH)3↓+3NH4+ |
下列说法正确的是(??)
| A、不含其他杂质的天然油脂属于纯净物 |
| B、肥皂的有效成分硬脂酸钠和甘油 |
| C、油脂的烃基部分饱和程度越大,熔点越低 |
| D、各种油脂水解后的产物中都有甘油 |
下列有机物的命名中,不正确的是( )
| A、3,3-二甲基丁烷 |
| B、3-甲基-3-乙基戊烷 |
| C、4-甲基-3-乙基-2-己烯 |
| D、1-甲基-2-乙基-3-丙基苯 |
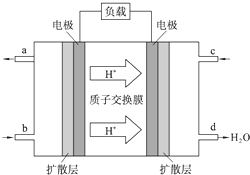 为了节能减排、缓解能源短缺,我国大力开发甲醇等可再生的新能源.工业上根据CO(g)+2H2(g)═CH3OH(g)△H合成甲醇.
为了节能减排、缓解能源短缺,我国大力开发甲醇等可再生的新能源.工业上根据CO(g)+2H2(g)═CH3OH(g)△H合成甲醇.