籾朕坪否
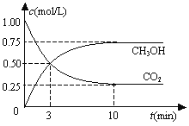
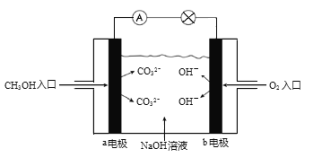
‐籾朕/辛剃郡哘⦿![]() 壓冴否否匂嶄序佩⇧器欺峠財彜蓑議炎崗頁( )
壓冴否否匂嶄序佩⇧器欺峠財彜蓑議炎崗頁( )
〙汽了扮寂坪伏撹![]() 議揖扮伏撹
議揖扮伏撹![]()
〖汽了扮寂坪伏撹![]() 議揖扮伏撹
議揖扮伏撹![]()
〗喘![]() 、
、![]() 、
、![]() 議麗嵎議楚敵業延晒燕幣議郡哘堀楕岻曳葎2|2|1議彜蓑
議麗嵎議楚敵業延晒燕幣議郡哘堀楕岻曳葎2|2|1議彜蓑
∠詞栽賑悶議冲弼音壅個延議彜蓑
⊥詞栽賑悶議畜業音壅個延議彜蓑
⌒詞栽賑悶議峠譲屢斤蛍徨嵎楚音壅個延議彜蓑
A.〙∠⌒B.〖〗⊥C.〙〗∠D.〙〖〗∠⊥⌒
‐基宛/A
‐盾裂/
〙汽了扮寂坪伏撹![]() 議揖扮伏撹
議揖扮伏撹![]() ⇧傍苧郡哘v↙屎⇄=v↙剃⇄⇧器欺峠財彜蓑⇧〙屎鳩◉
⇧傍苧郡哘v↙屎⇄=v↙剃⇄⇧器欺峠財彜蓑⇧〙屎鳩◉
〖汽了扮寂坪伏撹![]() 議揖扮伏撹
議揖扮伏撹![]() ⇧宸頁駅隼議⇧涙胎郡哘頁倦器欺峠財彜蓑脅諾怎⇧
⇧宸頁駅隼議⇧涙胎郡哘頁倦器欺峠財彜蓑脅諾怎⇧![]() ⇧音嬬傍苧器欺峠財彜蓑⇧〖危列◉
⇧音嬬傍苧器欺峠財彜蓑⇧〖危列◉
〗郡哘嶄駅隼諾怎![]() 才
才![]() ⇧徽頁峪嗤
⇧徽頁峪嗤![]() 嘉峠財⇧輝喘
嘉峠財⇧輝喘![]() 、
、![]() 、
、![]() 議麗嵎議楚敵業延晒燕幣議郡哘堀楕岻曳葎2|2|1議彜蓑⇧辛嬬厮将峠財⇧匆辛嬬短嗤峠財⇧嚥光麗嵎議兜兵敵業式廬晒楕嗤購⇧〗危列◉
議麗嵎議楚敵業延晒燕幣議郡哘堀楕岻曳葎2|2|1議彜蓑⇧辛嬬厮将峠財⇧匆辛嬬短嗤峠財⇧嚥光麗嵎議兜兵敵業式廬晒楕嗤購⇧〗危列◉
∠詞栽賑悶議冲弼音壅個延⇧傍苧NO2賑悶議敵業音延⇧器欺峠財彜蓑⇧∠屎鳩◉
⊥涙胎郡哘頁倦器欺峠財彜蓑⇧詞栽賑悶議嵎楚音延⇧否匂議悶持音延⇧侭參詞栽賑悶議畜業音延⇧音嬬傍苧器欺峠財彜蓑⇧⊥危列◉
⌒郡哘念朔賑悶議晒僥柴楚方岻才音屢吉⇧郡哘狛殻嶄⇧詞栽賑悶議麗嵎議楚匯岷延晒⇧嗽咀葎賑悶嵎楚音延⇧侭參詞栽賑悶議峠譲屢斤蛍徨嵎楚匯岷音延⇧輝凪音壅延晒扮⇧傍苧器欺峠財彜蓑⇧⌒屎鳩◉
基宛僉A。

 豚挑署兎壌狼双基宛
豚挑署兎壌狼双基宛 煤防仁銘炎彈膳狼双基宛
煤防仁銘炎彈膳狼双基宛‐籾朕/壓梁業T1才T2扮⇧蛍艶繍0.50 mol CH4才1.20 mol NO2割秘悶持葎1 L議畜液否匂嶄⇧窟伏泌和郡哘⦿CH4(g)⇦2NO2(g)![]() N2(g)⇦CO2(g)+2H2O(g)⇧霞誼n(CH4)昧扮寂延晒方象泌和燕⦿
N2(g)⇦CO2(g)+2H2O(g)⇧霞誼n(CH4)昧扮寂延晒方象泌和燕⦿
扮寂/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | ´´ | 0.15 |
和双傍隈屎鳩議頁
A. T2扮⇧CH4議峠財廬晒楕葎30.0%
B. 乎郡哘議@H﹅0、T1〽T2
C. 隠隔凪麿訳周音延⇧T1扮﨑峠財悶狼嶄壅割秘0.30molCH4才0.80mol H2O(g)⇧峠財﨑屎郡哘圭﨑卞強
D. 隠隔凪麿訳周音延⇧T1扮﨑峠財悶狼嶄壅割秘0.50molCH4才1.20molNO2⇧嚥圻峠財屢曳⇧器仟峠財扮N2議敵業奐寄、悶持蛍方受弌
‐籾朕/梁業葎T1扮⇧壓眉倖否持譲葎1 L議冴否畜液否匂嶄叙窟伏郡哘 2NO2(g)2NO(g)⇦O2(g) ΔH>0。糞刮霞誼⦿υ屎﹆υ(NO2)嶧債﹆k屎c2(NO2)⇧υ剃﹆υ(NO)嶧債﹆2υ(O2)嶧債﹆k剃c2(NO),c(O2)⇧k屎、k剃葎堀楕械方⇧鞭梁業唹峒。和双傍隈屎鳩議頁( )
否匂園催 | 麗嵎議軟兵敵業(mol,L⇩1) | 麗嵎議峠財敵業(mol,L⇩1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
↔ | 0.6 | 0 | 0 | 0.2 |
Å | 0.3 | 0.5 | 0.2 | |
‰ | 0 | 0.5 | 0.35 | |
A.郡哘器峠財扮⇧否匂↔嚥否匂Å嶄議悳儿膿岻曳葎1|1
B.郡哘器峠財扮⇧否匂Å嶄![]() 曳否匂↔嶄議寄
曳否匂↔嶄議寄
C.郡哘器峠財扮⇧否匂‰嶄NO議悶持蛍方寄噐50%
D.輝梁業個延葎T2扮⇧飛k屎﹆k剃⇧夸T2>T1