题目内容
【题目】温度为T1时,在三个容积均为1 L的恒容密闭容器中仅发生反应 2NO2(g)2NO(g)+O2(g) ΔH>0。实验测得:υ正=υ(NO2)消耗=k正c2(NO2),υ逆=υ(NO)消耗=2υ(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是( )
容器编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A.反应达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为1∶1
B.反应达平衡时,容器Ⅱ中![]() 比容器Ⅰ中的大
比容器Ⅰ中的大
C.反应达平衡时,容器Ⅲ中NO的体积分数大于50%
D.当温度改变为T2时,若k正=k逆,则T2>T1
【答案】D
【解析】
A.容器I中的反应
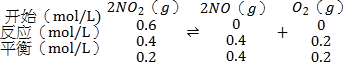
化学平衡常数K=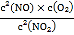 =
=![]() =0.8;
=0.8;
容器II中开始时浓度商Qc=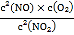 =
=![]() =
=![]() <0.8,则反应正向进行,平衡时混合气体的物质的量浓度之和大于1mol/L,所以达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比小于0.8mol/L:1mol/L=4:5,故A错误;
<0.8,则反应正向进行,平衡时混合气体的物质的量浓度之和大于1mol/L,所以达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比小于0.8mol/L:1mol/L=4:5,故A错误;
B.容器I中反应平衡时c(O2)=c(NO2),如果容器II中平衡时 c(NO2)=c(O2),设参加反应的 c(NO2)=xmol/L,则0.3-x=0.2+0.5x,解得x=![]() ,平衡时 c(NO2)=c(O2)=
,平衡时 c(NO2)=c(O2)=![]() mol/L,c(NO)=0.5mol/L+
mol/L,c(NO)=0.5mol/L+![]() mol/L=
mol/L=![]() mol/L,II中Qc=
mol/L,II中Qc=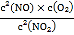 =
=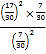 ≈1.4>0.8,说明II中平衡时应该存在 c(NO2)>c(O2),即容器Ⅱ中
≈1.4>0.8,说明II中平衡时应该存在 c(NO2)>c(O2),即容器Ⅱ中 ![]() <1,而容器I中
<1,而容器I中 ![]() =1,所以达平衡时,容器Ⅱ中
=1,所以达平衡时,容器Ⅱ中 ![]() 比容器Ⅰ中的小,故B错误;
比容器Ⅰ中的小,故B错误;
C.若容器Ⅲ在某时刻,NO的体积分数为50%,可得反应的三段式:
2NO2(g)2NO(g)+O2(g)
起始量(mol/L) 0 0.5 0.35
变化量(mol/L) 2y 2y y
平衡量(mol/L) 2y 0.5-2y 0.35-y
若0.5-2y=2y+0.35-y,解得y=0.05,求出此时浓度商Qc=![]() =4.8>K,说明此时反应未达平衡,反应继续向逆反应方向进行,NO进一步减少,平衡时NO的体积分数小于50%,故C错误;
=4.8>K,说明此时反应未达平衡,反应继续向逆反应方向进行,NO进一步减少,平衡时NO的体积分数小于50%,故C错误;
D.υ正=υ(NO2 )消耗=k正c2(NO2 ),υ逆=υ(NO)消耗=2υ(O2 )消耗=k逆c2 (NO)c(O2 ),达到平衡状态时正逆反应速率相等,则k正c2(NO2 )=k逆c (NO)c(O2 ),T2时若k正=k逆,则c2(NO2 )=c2 (NO)c(O2 ),化学平衡常数K=1>0.8,该反应的正反应是吸热反应,升高温度平衡正向移动,化学平衡常数增大,则T2>T1,故D正确;
故答案为D。

 阅读快车系列答案
阅读快车系列答案【题目】在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g) ![]() Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法正确的是( )
A. 上述生成Ni(CO)4(g)的反应为吸热反应
B. 25 ℃时反应Ni(CO)4(g) ![]() Ni(s)+4CO(g)的平衡常数为0.5
Ni(s)+4CO(g)的平衡常数为0.5
C. 在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均0.5 mol/L,则此时v正>v逆
D. 80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol/L