题目内容
12.利用下列各组物质制备和收集少量相应气体,能采用如图实验装置的是( )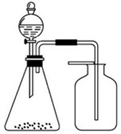
| A. | 浓氨水与固体CaO | B. | 稀盐酸与石灰石 | C. | 稀硝酸与铜片 | D. | 浓盐酸与MnO2 |
分析 图中装置制备气体的特点为:固体+固体不加热,制备气体用向上排空气法收集,则该气体密度大于空气密度,据此解答.
解答 解:A.氨气密度小于空气密度,应选择向下排空气法,故A错误;
B.稀盐酸与石灰石常温下反应生成二氧化碳,二氧化碳密度大于空气密度,应选择向上排气法收集,故B正确;
C.一氧化氮及易与空气反应生成二氧化氮,不能用排气法收集,故C错误;
D.浓盐酸与二氧化锰反应需要加热,不能用此装置制备,故D错误;
故选:B.
点评 本题考查常见气体的制备和收集,认真分析实验装置图的特点,熟知常见气体的制备原理和性质是解题的关键,题目难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
2.下列4个有机化合物中,能够发生酯化、加成和氧化3种反应的是( )
①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH2=CHCH2OH ④CH3CH2CH2OH⑤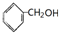
①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH2=CHCH2OH ④CH3CH2CH2OH⑤

| A. | ①③④ | B. | ②④ | C. | ①③⑤ | D. | ①②③⑤ |
3.现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)已知BA5为离子化合物,写出其电子式: .
.
(2)B元素基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
该同学所画的电子排布图违背了泡利原理.
(4)G位于ⅦB族d区,该元素的核外电子排布式为[Ar]3d54s2.
(5)检验F元素的方法是焰色反应,请用原子结构的知识解释产生此现象的原因:当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子.电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量.
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: |
| I1=738kJ•mol-1 I2=1 451kJ•mol-1 I3=7 733kJ•mol-1 I4=10 540kJ•mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
 .
.(2)B元素基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为

该同学所画的电子排布图违背了泡利原理.
(4)G位于ⅦB族d区,该元素的核外电子排布式为[Ar]3d54s2.
(5)检验F元素的方法是焰色反应,请用原子结构的知识解释产生此现象的原因:当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子.电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量.
20.对于元素周期表中下列位置的①~⑩十种元素,请回答有关问题(用元素符号或化学式回答):
(1)只需形成一个共价单键就能达到稳定结构的元素有H、F、Cl.
(2)气态氢化物溶于水呈碱性的化合物是NH3.
(3)⑩号元素最高正价含氧酸只具有共价键.
(4)彼此间形成共价化合物数量最多的两种元素分别是C、H.
(5)含氧量最高的共价化合物是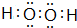 (用电子式表示).
(用电子式表示).
(6)①⑤⑦形成的化合物化学式为NaOH,含有的化学键类型是离子键、共价键.
(7)某元素气态氢化物为H2B,最高价氧化物含B的质量分数为40%,则气态氢化物的化学式为H2S,它与③形成的化合物的化学式为CS2,含有的化学键有共价键.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ||||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
(2)气态氢化物溶于水呈碱性的化合物是NH3.
(3)⑩号元素最高正价含氧酸只具有共价键.
(4)彼此间形成共价化合物数量最多的两种元素分别是C、H.
(5)含氧量最高的共价化合物是
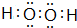 (用电子式表示).
(用电子式表示).(6)①⑤⑦形成的化合物化学式为NaOH,含有的化学键类型是离子键、共价键.
(7)某元素气态氢化物为H2B,最高价氧化物含B的质量分数为40%,则气态氢化物的化学式为H2S,它与③形成的化合物的化学式为CS2,含有的化学键有共价键.
7.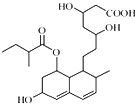 普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述正确的是( )
普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述正确的是( )
 普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述正确的是( )
普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述正确的是( )| A. | 能与FeCl3 溶液发生显色反应 | |
| B. | 能使酸性KMnO4 溶液褪色 | |
| C. | 能发生加成、取代,不能消去反应 | |
| D. | 1 mol 该物质最多可与1 mol NaOH 反应 |
17.已知化合物A的结构简式为 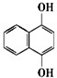 A苯环上的n溴代物的同分异构体的数目和m溴代物的同分异构体的数目相等,则n和m一定满足的关系式是( )
A苯环上的n溴代物的同分异构体的数目和m溴代物的同分异构体的数目相等,则n和m一定满足的关系式是( )
 A苯环上的n溴代物的同分异构体的数目和m溴代物的同分异构体的数目相等,则n和m一定满足的关系式是( )
A苯环上的n溴代物的同分异构体的数目和m溴代物的同分异构体的数目相等,则n和m一定满足的关系式是( )| A. | 2n=m | B. | n=m | C. | n+m=6 | D. | n+m=8 |
4.下列说法中正确的是( )
| A. | 随着原子序数的递增,第三周期元素的电负性逐渐减小 | |
| B. | 铝的第一电离能比镁的第一电离能大 | |
| C. | K、Na、Li的第一电离能逐渐增大 | |
| D. | 电负性差值大的元素原子之间形成的化学键主要是共价键 |
15.下列物质加热熔化时,所克服粒子间相互作用力属于同类型的是( )
| A. | 食盐和金属钠的熔化 | B. | 氯化铵和单质硫的熔化 | ||
| C. | 碘和干冰的升华 | D. | 金刚石和石灰石的熔化 |