题目内容
14.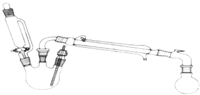 某研究性小组探究乙酸乙酯的反应机理,实验如下:已知:相关物理性质(常温常压)
某研究性小组探究乙酸乙酯的反应机理,实验如下:已知:相关物理性质(常温常压)| 密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 | |
| 乙醇 | 0.79 | -114 | 78 | 溶 |
| 乙酸 | 1.049 | 16.2 | 117 | 溶 |
| 乙酸乙酯 | 0.902 | -84 | 76.5 | 不溶 |
(1)制取乙酸乙酯化学方程式为:CH3COOH+CH3CH2OH
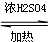 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.(2)浓硫酸与乙醇如何混合?先向三颈烧瓶加入乙醇,再沿着瓶壁缓慢加入浓硫酸,边振荡边滴加.
(3)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的是?保证乙醇量是乙酸量10倍以上,提高乙酸的转化率.
(5)蒸出的粗乙酸乙酯中主要有哪些杂质?乙醚、乙酸、乙醇和水.
(6)饱和的Na2CO3溶液洗涤除去乙酸,能否换成NaOH溶液?若不能,为什么?(用化学方程式表示)不能;CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH.用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,为什么不用水?减少乙酸乙酯溶解.
分析 (1)在浓硫酸作催化剂和加热条件下,乙酸与乙醇反应生成乙酸乙酯和水;
(2)从浓硫酸溶于水放热分析;
(3)液体加热要加碎瓷片,防止暴沸,忘记加瓷片,应该采取冷却后补加;
(4)乙酸乙酯的制备反应是可逆反应,为提高反应物的转化率和提高产率,通常采取增大某反应物的浓度或减小生产物的浓度的方法;
(5)根据该反应的特点以及发生的副反应解答;
(6)乙酸乙酯在强碱溶液中会发生水解;用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,减少乙酸乙酯溶解.
解答 解:(1)在浓硫酸作催化剂和加热条件下,乙酸与乙醇反应生成乙酸乙酯和水,其反应的方程式为:CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
故答案为:CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(2)为防止酸液飞溅,应将密度大的液体加入到密度小的液体中,应将浓硫酸加入到乙醇中,防止硫酸溶解时放出大量的热导致液体飞溅,
故答案为:先向三颈烧瓶加入乙醇,再沿着瓶壁缓慢加入浓硫酸,边振荡边滴加;
(3)液体乙酸乙醇沸点低,加入沸石(碎瓷片),可以通过孔隙凝聚蒸汽,使成为气泡浮出,防止暴沸,如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是冷却后补加,
故答案为:B;
(4)通过分液漏斗中边滴加乙酸和乙醇混和液边加热蒸馏,可以不断增大乙酸和乙醇混和液的浓度,减小乙酸乙酯的浓度,有利于平衡向正反应方向移动,控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的保证乙醇量是乙酸量10倍以上,提高乙酸的转化率,
故答案为:保证乙醇量是乙酸量10倍以上,提高乙酸的转化率;
(5)CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O该反应为可逆反应,同时有副反应2C2H5OH$→_{140℃}^{浓硫酸}$C2H5OC2H5+H2O,所以反应物和生成物共存,蒸出的粗乙酸乙酯中主要有乙醚、乙酸、乙醇和水;
CH3COOCH2CH3+H2O该反应为可逆反应,同时有副反应2C2H5OH$→_{140℃}^{浓硫酸}$C2H5OC2H5+H2O,所以反应物和生成物共存,蒸出的粗乙酸乙酯中主要有乙醚、乙酸、乙醇和水;
故答案为:乙醚、乙酸、乙醇和水;
(6)乙酸乙酯在强碱溶液中会发生水解,其反应为:CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH,所以不能用成NaOH溶液代替饱和的Na2CO3溶液;用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,可以减少乙酸乙酯溶解,如用水洗,导致产率降低;
故答案为:不能;CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH;减少乙酸乙酯溶解.
点评 本题考查实验室制备乙酸乙酯的方案设计与评价,题目难度较大,本题注意把握实验操作原理,把握题给信息,掌握实验操作方法,学习中注意积累.

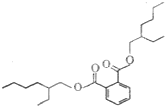 塑化剂是工业上被广泛使用的高分子材料添加剂,食用后对人体有害,其结构式如图.下列有关塑化剂的说法正确的是( )
塑化剂是工业上被广泛使用的高分子材料添加剂,食用后对人体有害,其结构式如图.下列有关塑化剂的说法正确的是( )| A. | 易溶于水,其水溶液有丁达尔效应 | B. | 在稀硫酸中不能稳定存在 | ||
| C. | 不能发生还原反应 | D. | 不能发生氧化反应 |
| A. | S.O.K | B. | Na.C.O | C. | H.O.S | D. | H.N.O |
①苯不能使溴的CCl4溶液褪色;②苯不能使酸性高锰酸钾溶液褪色;③苯在一定条件下既能发生取代反应,又能发生加成反应;④经测定,邻二甲苯只有一种结构;⑤苯的一氯代物只有一种.
| A. | ①②④⑤ | B. | ①②③⑤ | C. | ①②④ | D. | ①②③④ |
| A. | 煤的液化是物理变化 | |
| B. | 石油干馏可得到汽油、煤油等 | |
| C. | 淀粉、蛋白质完全水解的产物互为同分异构体 | |
| D. | 乙酸乙酯、油脂与NaOH溶液反应均有醇生成 |
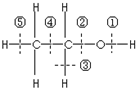 乙醇分子结构中各种化学键如图所示,工业上可用乙烯水化法制乙醇,下列关于对乙烯和乙醇的有关说法不正确的( )
乙醇分子结构中各种化学键如图所示,工业上可用乙烯水化法制乙醇,下列关于对乙烯和乙醇的有关说法不正确的( )| A. | 乙烯分子为平面结构 | |
| B. | 乙烯可用作植物生长的调节剂 | |
| C. | 乙醇在铜催化下和氧气反应键①和③断裂 | |
| D. | 乙醇和乙酸、浓硫酸共热时键②断裂 |
| A. | 2-乙基丁烷 | B. | 2-甲基戊烷 | C. | 3-甲基戊烷 | D. | 3-乙基丁烷 |
| A. | Na2O | B. | H2O | C. | HCl | D. | NaOH |
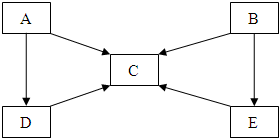 A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.其中A、B、C、D、E在常温下都是气体,B为红棕色.
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.其中A、B、C、D、E在常温下都是气体,B为红棕色.