题目内容
下列说法正确的是( )
| A、Na2SO3与BaCl2溶液作用,有白色沉淀,加稀硝酸后沉淀消失 |
| B、将SO2气体通入Ba(OH)2溶液中没有白色沉淀生成 |
| C、将SO2气体通过BaCl2溶液中有白色沉淀生成 |
| D、将SO2气体通入用硝酸酸化的BaCl2溶液中有白色沉淀生成 |
考点:二氧化硫的化学性质,含硫物质的性质及综合应用
专题:氧族元素
分析:A.白色沉淀为亚硫酸钡,与硝酸发生氧化还原反应;
B.反应生成亚硫酸钡和水;
C.SO2气体通过BaCl2溶液中不反应;
D.SO2气体通入用硝酸酸化的BaCl2溶液中,先发生氧化还原反应生成硫酸根离子,再与钡离子反应.
B.反应生成亚硫酸钡和水;
C.SO2气体通过BaCl2溶液中不反应;
D.SO2气体通入用硝酸酸化的BaCl2溶液中,先发生氧化还原反应生成硫酸根离子,再与钡离子反应.
解答:
解:A.白色沉淀为亚硫酸钡,与硝酸发生氧化还原反应,则生成硫酸钡白色沉淀,故A错误;
B.反应生成亚硫酸钡和水,有白色沉淀生成,故B错误;
C.SO2气体通过BaCl2溶液中不反应,没有白色沉淀生成,故C错误;
D.SO2气体通入用硝酸酸化的BaCl2溶液中,先发生氧化还原反应生成硫酸根离子,再与钡离子反应,生成硫酸钡白色沉淀,故D正确;
故选D.
B.反应生成亚硫酸钡和水,有白色沉淀生成,故B错误;
C.SO2气体通过BaCl2溶液中不反应,没有白色沉淀生成,故C错误;
D.SO2气体通入用硝酸酸化的BaCl2溶液中,先发生氧化还原反应生成硫酸根离子,再与钡离子反应,生成硫酸钡白色沉淀,故D正确;
故选D.
点评:本题考查二氧化硫的化学性质,为高频考点,把握二氧化硫的酸性氧化物性质及还原性为解答的关键,注意发生的氧化还原反应,题目难度不大.

练习册系列答案
相关题目
用如图装置实验,下列叙述不正确的是( )
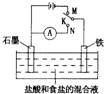

| A、K与N连接时,组成原电池装置 |
| B、K与N连接时,石墨电极产生气泡 |
| C、K与M连接时,一段时间后溶液的pH减小 |
| D、K与M连接时,石墨电极的反应为:2Cl--2e-═Cl2↑ |
下列反应的离子方程式正确的是( )
| A、NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B、往碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O |
| C、氧化铜溶于浓硝酸:CuO+2H+=Cu2++2H2O |
| D、向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
X、Y、Z、W、Q均为含氮的化合物,在一定条件下,将发生如下转换关系(未配平):
①X→W+O2
②Z+Y+NaOH→H2O+W
③Y+SO2→Z+SO3
④Q+Y→Z+H2O
⑤X+Cu+H2SO4→Cu2++Y+SO42-
这五种化合物中氮元素的化合价由高到低的顺序为( )
①X→W+O2
②Z+Y+NaOH→H2O+W
③Y+SO2→Z+SO3
④Q+Y→Z+H2O
⑤X+Cu+H2SO4→Cu2++Y+SO42-
这五种化合物中氮元素的化合价由高到低的顺序为( )
| A、XYZWQ |
| B、XZYQW |
| C、XYWZQ |
| D、WXZQY |
将51.2g铜恰好完全溶于一定量的硝酸溶液中,得到硝酸铜溶液,收集到氮的氧化物(含NO、NO2、N2O4)的混合物共17.92L(标准状况),在这些气体中通入V L(标准状况)的氧气后用一定量的氢氧化钠溶液吸收,结果剩余2.24L(标准状况)气体.则通入氧气的体积V为( )
| A、7.28L |
| B、8.96L |
| C、11.20L |
| D、16.8L |
在Na与H2O的反应中( )
| A、Na是氧化剂 |
| B、反应实质是钠置换水中的氢气 |
| C、反应实质是钠置换水电离出的少量的H+ |
| D、H2是氧化产物 |