题目内容
【题目】将14.2g Na2SO4完全溶于水中,配成500 mL溶液,其物质的量浓度为__________;若从中取出50 mL,Na+物质的量浓度为___________;若将这50 mL溶液用水稀释至100 mL,所得溶液中SO42-的物质的量浓度为___________。
【答案】 0.2 mol·L-1 0.4 mol·L-1 0.1 mol·L-1
【解析】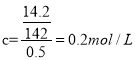 ,取出的溶液中;硫酸钠的浓度也是0.2mol/L,所以钠离子浓度为0.4mol/L。将这50 mL溶液用水稀释至100 mL,溶液体积变为原来的二倍,浓度应该变为原来的0.5倍。原溶液为0.2mol/L的硫酸钠,硫酸根离子浓度为0.2mol/L,所稀释后为0.1mol/L。
,取出的溶液中;硫酸钠的浓度也是0.2mol/L,所以钠离子浓度为0.4mol/L。将这50 mL溶液用水稀释至100 mL,溶液体积变为原来的二倍,浓度应该变为原来的0.5倍。原溶液为0.2mol/L的硫酸钠,硫酸根离子浓度为0.2mol/L,所稀释后为0.1mol/L。

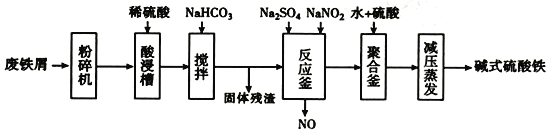
【题目】(1)银作为催化剂,主要用于乙烯氧化制环氧乙烷、甲醇氧化制甲醛等。目前银催化剂的市场需求呈逐年增加的趋势。请写出甲醇在银催化下制备甲醛的化学方程式
________________________________________________________________。
(2)银催化剂在使用过程中,催化活性逐渐减弱、选择性降低,一定时间后必须更换。某工厂对失效银催化剂进行回收并实现再生,工艺流程如下:

已知:银催化剂主要成分(X射线荧光光谱法分析)
元素 | Al2O3 | Ag | MgO | SiO2 | K2O | Fe2O3 |
含量% | 82 | 14.8 | 1.4 | 0.9 | 0.5 | 0.1 |
资料:经X射线衍射仪检测,其中氧化铝的晶型为α型,难于酸。
①操作a和操作b的名称是_________。
②请写出过程Ⅰ中银与稀硝酸反应的离子方程式
________________________________________________________________。
(3)滤液2 中含有多种金属离子,请简述检验其中K+的实验方法
____________________________________________________________________。
(4)结合化学用语从平衡移动角度解释过程Ⅲ中用氨水将氯化银沉淀溶解的原
因_______________________________________________________________。
(5)过程Ⅳ采用肼(N2H4)作为还原剂,具有不混入金属杂质、还原性强、得到银纯度高等优点,该过程的化学方程式为:
________________________________________________________。
(6)利用过程Ⅴ实现银催化剂再生,其简易装置图如下:

写出催化剂再生的电极反应式:________________________________。