题目内容
3.为探究离子反应的实质,某同学设计了如下实验,有关的实验现象及反应方程式列表如下:(1)填充表:
| 编号 | I | II | III |
| 实验 | 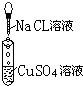 | 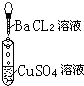 |  |
| 现象 | 有白色沉淀生成,滤液为蓝色 | 有白色沉淀生成,滴加稀硝酸,沉淀不溶解 | |
| 化学方程式 | 2AgNO3+CuCl2═2AgCl↓+Cu(NO3)2 | ||
| 离子方程式 | Ba2++SO42-═BaSO4↓ |
分析 (1)氯化钠与硫酸铜不发生反应,溶液仍为蓝色;氯化钡与硫酸铜溶液反应生成硫酸钡沉淀和氯化铜;硝酸银溶液与氯化铜溶液反应生成氯化银沉淀和硝酸铜,据此写出反应的化学方程式或离子方程式;
(2)实验II反应后的溶液中还有的离子有:氯离子、铜离子、氢离子、氢氧根离子、钡离子、硫酸根离子;滤液为蓝色,证明铜离子没有反应.
解答 解:(1)氯化钠与硫酸铜溶液不发生反应,则没有明显现象;
氯化钡与硫酸铜溶液反应生成硫酸钡沉淀和氯化铜,反应的化学方程式为:BaCl2+CuSO4═BaSO4↓+CuCl2,离子方程式为Ba2++SO42-═BaSO4↓;
硝酸银与氯化铜溶液反应生成氯化银沉淀,反应的化学方程式为:2AgNO3+CuCl2═2AgCl↓+Cu(NO3)2,离子方程式为Ag++Cl-=AgCl↓,
故答案为:
| 编号 | I | II | III |
| 实验 | |||
| 现象 | 没有明显变化,溶液仍为蓝色 | ||
| 化学方程式 | 无 | BaCl2+CuSO4═BaSO4↓+CuCl2 | |
| 离子方程式 | 无 | Ag++Cl-=AgCl↓ |
(2)实验II反应后的溶液中还有的离子有:氯离子、铜离子、氢离子、氢氧根离子、钡离子、硫酸根离子,总共有6种;根据反应后的溶液为蓝色可知铜离子没有参与反应,
故答案为:6;滤液为蓝色.
点评 本题探究了化学反应机理,题目难度中等,明确发生反应实质为解答关键,试题侧重考查学生的分析、理解能力及化学实验能力.

练习册系列答案
相关题目
11.下列离子方程式不正确的是( )
| A. | Fe3O4与稀HNO3反应的离子方程式为:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| B. | 用稀H2SO4除去铜绿:4H++Cu2(OH)2CO3═2Cu2++CO2↑+3H2O | |
| C. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓ | |
| D. | 少量Ca(OH)2溶液与NaHCO3混合:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- |
18.葡萄糖能够和银氨溶液发生银镜反应,主要是它含有( )
| A. | 羟基 | B. | 双键 | C. | 醛基 | D. | 酯基 |
8.下列说法正确的是( )
| A. | 常温下,0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合,测得混合溶液pH=8,则混合溶液中水电离产生的c(OH-)=1×10-8 | |
| B. | 室温下,CH3COONa和CaCl2的混合溶液:c (Na+)+c(Ca2+)=c (CH3COO-)+c(CH3COOH)+c(Cl-) | |
| C. | 恒容密闭容器中进行反应2A2(g)+B2(g)?2A2B(g)△H<0,达到化学平衡后,加热会使逆反应速率大于正反应速率 | |
| D. | 常温下,pH=11的氨水和pH=1的盐酸等体积混合,恰好完全反应,则混合溶液中c(NH4+)+c(NH3?H2O)+c(NH3)=5×10-4mol/L |
12.X、Y都是芳香族化合物,1molX水解得到1molY和2mol醋酸.Y相对分子质量介于100~150之间,且碳和氢两种元素总质量分数为65.2%.X溶液能发生银镜反应,向Y水溶液中滴加NaHCO3无气泡,滴加FeCl3溶液显紫色.下列说法正确的是( )
| A. | X、Y相对分子质量之差为84 | |
| B. | X中含有HCOO-,Y中含有-OH | |
| C. | Y的分子式为:C7H8O3 | |
| D. | 若X中有四种氢,则满足条件的X可能有两种 |

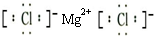 .
.