题目内容
13.区别H2和CO可用的方法是( )①点燃后,观察火焰的颜色;②点燃后,在火焰上方罩一冷而干燥的小烧杯;③将燃烧产物通入石灰水中;④与灼热的氧化铜反应.
| A. | ①②③④ | B. | ②③ | C. | ③④ | D. | ②③④ |
分析 H2和CO均具有还原性,但还原产物不同,且二者均易燃烧,且燃烧产物不同,以此来解答.
解答 解:①点燃后,均观察到淡蓝色火焰的颜色,现象相同,故不选;
②点燃后,在火焰上方罩一冷而干燥的小烧杯,氢气燃烧可观察到内壁有水,现象不同,可鉴别,故选;
③将燃烧产物通入石灰水中,CO的燃烧产物能使石灰水变浑浊,现象不同,可鉴别,故选;
④均能与灼热的氧化铜反应,但还原产物不同,不检验还原产物不能鉴别,故不选;
故选B.
点评 本题考查物质的鉴别,为高频考点,把握物质的性质、性质差异及反应为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
3.下列选项中最后的物质是要制取的物质,其中不可能得到的是( )
| A. | CaCO3$\stackrel{高温}{→}$CaO$\stackrel{H_{2}O}{→}$Ca(OH)2$→_{过滤}^{Na_{2}CO_{3}}$NaOH溶液 | |
| B. | Cu$→_{△}^{O_{2}}$CuO$→_{△}^{H_{2}SO_{4}}$CuSO4溶液$→_{过滤}^{NaOH溶液}$Cu(OH)2沉淀 | |
| C. | KMnO4$\stackrel{△}{→}$O2$\stackrel{点燃S}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4溶液 | |
| D. | BaCO3$\stackrel{盐酸}{→}$BaCl2溶液$\stackrel{通入H_{2}SO_{4}}{→}$BaSO4沉淀 |
4.配制一定物质的量浓度的NaOH溶液时,造成实验结果偏低的是( )
| A. | 未冷却至室温直接把NaOH溶液移入容量瓶中 | |
| B. | 定容时观察液面仰视 | |
| C. | 样品中含有少量Na2O杂质 | |
| D. | 容量瓶中原来有少量蒸馏水 |
1.下列叙述中,前者是化学变化,后者是物理变化的是( )
| A. | 燃烧、汽化 | B. | 发光、着火点 | C. | 挥发性、导电性 | D. | 易燃性、自燃 |
8.下列反应中,不属于置换反应的是( )
| A. | Fe+CuSO4═FeSO4+Cu | B. | CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | ||
| C. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | D. | Fe+2HCl═FeCl2+H2↑ |
18.下列实验中,①pH试纸的使用 ②过滤 ③蒸发,均用到的仪器是( )
| A. | 蒸发皿 | B. | 玻璃棒 | C. | 试管 | D. | 分液漏斗 |
2.下列关于摩尔的说法中正确的是( )
| A. | 摩尔是一个物理量,是6.02×1023个粒子、 | |
| B. | 摩尔是物质质量的单位 | |
| C. | 摩尔是表示物质的量的单位 | |
| D. | 摩尔的标准是0.12kg12C中所含有的原子数目 |
3.为探究离子反应的实质,某同学设计了如下实验,有关的实验现象及反应方程式列表如下:
(1)填充表:
(2)实验II反应后的溶液中还有离子种类有6,能证明Cu2+没有参与反应的实验现象是滤液为蓝色.
(1)填充表:
| 编号 | I | II | III |
| 实验 | 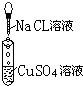 | 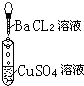 |  |
| 现象 | 有白色沉淀生成,滤液为蓝色 | 有白色沉淀生成,滴加稀硝酸,沉淀不溶解 | |
| 化学方程式 | 2AgNO3+CuCl2═2AgCl↓+Cu(NO3)2 | ||
| 离子方程式 | Ba2++SO42-═BaSO4↓ |