题目内容
11.下列离子方程式不正确的是( )| A. | Fe3O4与稀HNO3反应的离子方程式为:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| B. | 用稀H2SO4除去铜绿:4H++Cu2(OH)2CO3═2Cu2++CO2↑+3H2O | |
| C. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓ | |
| D. | 少量Ca(OH)2溶液与NaHCO3混合:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- |
分析 A.发生氧化还原反应生成硝酸铁、NO和水;
B.反应生成硫酸铜、二氧化碳和水;
C.恰好使SO42-完全沉淀,以1:2反应生成硫酸钡、氢氧化铝和一水合氨;
D.少量Ca(OH)2完全反应,反应生成碳酸钙、碳酸钠和水.
解答 解:A.Fe3O4与稀HNO3反应的离子方程式为3Fe3O4+NO3-+28H+═9Fe3++NO↑+14H2O,故A错误;
B.用稀H2SO4除去铜绿的离子反应为4H++Cu2(OH)2CO3═2Cu2++CO2↑+3H2O,故B正确;
C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀的离子反应为2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓,故C正确;
D.少量Ca(OH)2溶液与NaHCO3混合的离子反应为Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32-,故D正确;
故选A.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.下列叙述中,前者是化学变化,后者是物理变化的是( )
| A. | 燃烧、汽化 | B. | 发光、着火点 | C. | 挥发性、导电性 | D. | 易燃性、自燃 |
2.下列关于摩尔的说法中正确的是( )
| A. | 摩尔是一个物理量,是6.02×1023个粒子、 | |
| B. | 摩尔是物质质量的单位 | |
| C. | 摩尔是表示物质的量的单位 | |
| D. | 摩尔的标准是0.12kg12C中所含有的原子数目 |
19.下列有关化学用语表示正确的是( )
| A. | CH4分子的球棍模型: | B. | 聚氯乙烯的结构简式为CH2CHCl | ||
| C. | 3,3-二甲基-1-戊烯的键线式: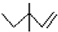 | D. | 乙醇分子的比例模型: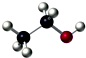 |
6.在实验室配制0.10mol•L-1的KCl溶液,下列操作会导致所配溶液浓度偏高的是( )
| A. | 转移溶液时使用的烧杯未洗涤 | B. | 定容时俯视读取刻度线 | ||
| C. | 原容量瓶洗净后未干燥 | D. | 转移时有少量溶液流出瓶外 |
16.硼酸溶液中存在如下反应:H3BO3(aq)+H2O(l)?[B(OH)4]-(aq)+H+(aq),下列说法正确的是( )
| 化学式 | 电离常数(298K) |
| H3BO3 | K=5.7×10-10 |
| H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
| CH3COOH | K=1.75×10-5 |
| A. | 等物质的量浓度的硼酸溶液和碳酸氢钠溶液比较,pH:后者>前者 | |
| B. | 等物质的量浓度的碳酸溶液和硼酸溶液比较,pH:前者>后者 | |
| C. | 将一滴醋酸溶液滴入碳酸钠溶液中一定能观察到有气泡产生 | |
| D. | 将一滴碳酸钠溶液滴入硼酸溶液中一定能观察到有气泡产生 |
3.为探究离子反应的实质,某同学设计了如下实验,有关的实验现象及反应方程式列表如下:
(1)填充表:
(2)实验II反应后的溶液中还有离子种类有6,能证明Cu2+没有参与反应的实验现象是滤液为蓝色.
(1)填充表:
| 编号 | I | II | III |
| 实验 | 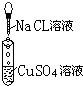 | 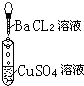 |  |
| 现象 | 有白色沉淀生成,滤液为蓝色 | 有白色沉淀生成,滴加稀硝酸,沉淀不溶解 | |
| 化学方程式 | 2AgNO3+CuCl2═2AgCl↓+Cu(NO3)2 | ||
| 离子方程式 | Ba2++SO42-═BaSO4↓ |
20.有Na2CO3,Ba(OH)2,H2SO4三种体积和物质的量浓度都相等的溶液,几位同学按不同的顺序将它们混合(产生沉淀立即过滤掉),对于所得溶液,下列结论正确的是( )
| A. | 溶液一定显碱性 | B. | 溶液不可能显碱性 | ||
| C. | 溶液可能显碱性 | D. | 溶液不可能显酸性 |