题目内容
19.下列说法正确的是( )| A. | 碱性氧化物一定是金属氧化物,但酸性氧化物不一定都是非金属氧化物 | |
| B. | 胶体会产生电泳现象是因为胶体吸附带电离子而显电性 | |
| C. | 电解质与非电解质的本质区别是水溶液能否导电 | |
| D. | 离子反应是否能够发生要看离子之间能否发生复分解反应 |
分析 A、碱性氧化物一定是金属氧化物,酸性氧化物可以是金属氧化物;
B、胶体中的胶粒在外加电源的作用下会发生定向移动是由于胶体粒子具有较大的表面积,是胶体的电泳现象;
C、电解质是指在水溶液中或熔融状态下能导电的化合物,非电解质指的是在水溶液中和熔融状态下均不能导电的化合物;
D、发生离子反应的条件是发生复分解反应,氧化还原反应,络合反应等.
解答 解:A、碱性氧化物一定是金属氧化物,酸性氧化物可以是金属氧化物,如:Mn2O7是酸性氧化物,故A正确;
B、胶体粒子具有较大的表面积,能吸附阳离子或阴离子,所以胶体具有吸附性,胶体的胶粒吸附胶体中带电荷的离子带电,如氢氧化铁胶体的胶粒吸附三价铁离子,带正电荷,通电后,氢氧化铁胶体的胶粒向阴极移动,产生电泳现象,故B正确;
C、电解质是指在水溶液中或熔融状态下能导电的化合物,非电解质指的是在水溶液中和熔融状态下均不能导电的化合物,两者的本质区别是在水溶液中和熔融状态下本身能否电离出自由移动的离子而导电,与水溶液是否导电无必然联系,故C错误;
D、离子反应是否能够发生要看离子之间能否发生复分解反应,氧化还原反应,络合反应等,故D错误;
故选AB.
点评 本题考查了化学概念和物质分类的理解应用,主要是电解质、非电解质、胶体,氧化物的概念实质分析,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
10.在一个固定体积的密闭容器中,加入2molA和1molB,发生反应 2A(g)+B(g)?2C(g),达到平衡时,C的物质的量浓度为K mol/L,若维持容器体积和温度不变,按下列配比作为起始物质.达到平衡后,C的物质的量浓度仍是K mol/L的是( )
| A. | 4molA+2molB | B. | 2molA+1molB+2molC | ||
| C. | 2molC+1molB | D. | 1molA+0.5molB+1molC |
11.既能与酸(H+)反应,又能与碱(OH-)反应的是( )
①MgO ②Al ③NaHSO4 ④NaHCO3 ⑤CaCO3.
①MgO ②Al ③NaHSO4 ④NaHCO3 ⑤CaCO3.
| A. | ②④ | B. | ②③④ | C. | ②④ | D. | ②④③ |
8.2014年8月2日江苏昆山某公司汽车轮毂抛光车间在生产过程中发生爆炸,经调查分析是铝粉遇明火引发爆炸.下列有关说法不正确的是( )
| A. | 活泼的金属粉尘遇明火均易引起爆炸 | |
| B. | 任何金属粉末在不正确操作下均可能引起爆炸 | |
| C. | 汽车轮毂表面镀铝既增加美观度,又耐腐蚀 | |
| D. | 事故告诫人们安全生产,防污、防爆非常重要 |
4.将0.5mol Cu2S与足量稀HNO3反应,生成Cu(NO3)2、S、NO和H2O.下列说法正确的是( )
| A. | Cu2S在反应中既是氧化剂又是还原剂 | |
| B. | 以上反应中转移电子的物质的量为1 mol | |
| C. | 以上参加反应的HNO3中被还原的HNO3为2 mol | |
| D. | 反应中,氧化剂和还原剂的物质的量之比为4:3 |
10.部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共2.88g,经如下处理:

下列说法错误的是( )

下列说法错误的是( )
| A. | 滤液A中不含Fe3+ | |
| B. | 样品中含氧元素的物质的量为0.01mol | |
| C. | 上图中V=112 | |
| D. | 溶解样品的过程中消耗的硫酸的总的物质的量为0.02mol |
4.100ml 2mol/L的稀硫酸与过量的锌片反应,为加快反应速率,又不影响氢气的总量,可采用的方法是( )
| A. | 不用稀硫酸,改用98%浓硫酸 | B. | 加入更多锌片 | ||
| C. | 加入适量的氯化钠溶液 | D. | 加入数滴氯化铜溶液 |
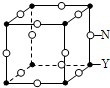 原子序数依次增大的X、Y、Z、M、N五种元素,XZ2是引起温室效应的主要气体,M最外层电子数是电子层数的2倍,N2+核外3d有9个电子,请回答下列问题:
原子序数依次增大的X、Y、Z、M、N五种元素,XZ2是引起温室效应的主要气体,M最外层电子数是电子层数的2倍,N2+核外3d有9个电子,请回答下列问题: