题目内容
【题目】图中表示2NO(g)+O2(g)![]() 2NO2(g)△H<0,能正确反映该可逆反应变化的图象是( )
2NO2(g)△H<0,能正确反映该可逆反应变化的图象是( )
A. 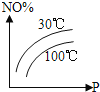 B.
B. 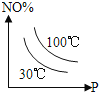
C. 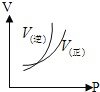 D.
D. 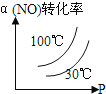
【答案】B
【解析】
2NO(g)+O2(g)![]() 2NO2(g)△H<0,反应为正反应气体体积增大的放热反应,据勒夏特列原理分析。
2NO2(g)△H<0,反应为正反应气体体积增大的放热反应,据勒夏特列原理分析。
反应为正反应气体体积增大的放热反应,
A、随压强增大,平衡向体积减小的正反应方向移动,NO含量应减小,故A错误;
B、随压强增大,平衡向体积减小的正反应方向移动,NO含量减小,随温度升高,平衡向吸热的逆反应方向移动,NO含量增大,故B正确;
C、随压强增大正逆反应速率都增大,但正反应速率比逆反应速率增大的快,故C错误;
D、随压强增大,平衡向体积减小的正反应方向移动,NO转化率增大,但随温度升高,平衡向吸热的逆反应方向移动,NO转化率降低,故D错误;
故选:B。

 全优点练单元计划系列答案
全优点练单元计划系列答案【题目】2019年10月27日,国际清洁能源会议(ICCE2019)在北京开幕。一碳化学成为这次会议的重要议程。甲醇、甲醛(HCHO) 等一碳化合物在化工 、医药,能源等方面都有着广泛的应用。
(1)甲醇脱氢法可制备甲醛(反应体系中各物质均为气态),反应生成 1mol HCHO过程中能量变化如图1。

已知:CO2(g)+3H2(g)=CH3OH(g) +H2O(g) △H=-49.5kJ mo1-1,则反应CO2(g)+2H2(g)= HCHO(g) +H2O(g) △H= ___________kJ mo1-1。
(2)氧化剂可处理甲醛污染,结合图2分析春季(水温约为15℃)应急处理被甲醛污染的水源应选择的试剂为__________(填化学式)。

(3)纳米二氧化钛催化剂可用于工业上合成甲醇,CO2(g)+2H2(g)![]() CH3OH(g) △H=akJmo1-1
CH3OH(g) △H=akJmo1-1
①按![]() =2,投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应测定CO的平衡转化率与温度、压强的关系如图3所示。则a _____(填“>”或“<”)0;压强p1、p2、p3由小到大的关系是__________________。
=2,投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应测定CO的平衡转化率与温度、压强的关系如图3所示。则a _____(填“>”或“<”)0;压强p1、p2、p3由小到大的关系是__________________。

②在温度为T1℃,向某恒容密闭容器中充入 H2和CO发生上述反应,起始时c(H2)=c(CO)=2.0 mo1L-1。达到平衡时,CO的转化率为图3中的 M 点对应的转化率,则在该温度下,对应的N 点的平衡常数为__________(保留3 位有效数字)。
(4)工业上利用CH4(CO和H2)与水蒸气在一定条件下制取 H2:CH4(g) +H2O(g)![]() CO(g)+3H2(g) △H=+203kJmo1-1,该中反应的逆反应速率及表达式为v逆=kc(CO)c3(H2),k 为速率常数,在某温度下测得实验数据如表所示,
CO(g)+3H2(g) △H=+203kJmo1-1,该中反应的逆反应速率及表达式为v逆=kc(CO)c3(H2),k 为速率常数,在某温度下测得实验数据如表所示,
CO浓度(mo1L-1) | H2浓度(mo1L-1) | 逆反应速率(mo1L-1min-1) |
0.1 | c1 | 8.0 |
c2 | c1 | 16.0 |
c2 | 0.15 | 6.75 |
由上还数据可得该温度下,c2=____________,该反应的逆反应速率常数 k=______L3mo1-3min-1)。