题目内容
【题目】中学化学中下列各物质间不能实现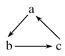 (“→”表示一步完成)转化的是
(“→”表示一步完成)转化的是
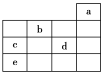
选项 | A | B | C | D |
a | CH3CH2OH | CH2=CH2 | Cl2 | C |
b | CH3CHO | CH3CH2Br | HClO | CO |
c | CH3COOH | CH3CH2OH | HCl | CO2 |
A. AB. BC. CD. D
【答案】A
【解析】
A、乙酸不能转变成乙醛,乙醛还原得到乙醇,乙醇氧化得到乙酸,故A错误;B、乙烯与溴化氢发生加成反应得到氯乙烷,溴乙烷水解得到乙醇,乙醇发生消去反应得到乙烯,故B正确;C、氯气与水反应生成次氯酸和盐酸,次氯酸分解产生盐酸和氧气,浓盐酸与二氧化锰反应生成氯气,故C正确;D、碳不完全燃烧生成一氧化碳,一氧化碳继续燃烧生成二氧化碳,二氧化碳与镁反应生成氧化镁和单质碳,故D正确;故选:A。

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目