题目内容
3.X、Y、Z为短周期元素,X的单质与水在常温条件下就能剧烈反应生成一种还原性气体,Y的最高价氧化物对应的水化物是一种酸性最强的酸;Z与Y同周期且只能形成ZY3;X、Z的简单离子核外电子排布相同.下列有关叙述正确的是( )| A. | 离子半径:X>Y>Z | B. | 最外层电子数:Y>Z>X | ||
| C. | 原子序数:Z>Y>X | D. | 单质熔点:X>Z>Y |
分析 X、Y和Z是第三周期的三种元素,X的单质与水在常温条件下就能剧烈反应生成一种还原性气体,则X为Na元素;Y的最高价氧化物对应的水化物是一种酸性最强的酸,则Y为Cl元素;Z与Y同周期且只能形成ZY3,则Z只能为Al元素,其铝离子与钠离子具有相同的电子排布,据此结合元素周期律知识对各选项进行判断.
解答 解:X、Y和Z是第三周期的三种元素,X的单质与水在常温条件下就能剧烈反应生成一种还原性气体,则X为Na元素;Y的最高价氧化物对应的水化物是一种酸性最强的酸,则Y为Cl元素;Z与Y同周期且只能形成ZY3,则Z只能为Al元素,其铝离子与钠离子具有相同的电子排布,
A.离子的电子层越多,离子半径越大,电子层相同时,离子的核电荷数越大,离子半径越小,则离子半径大小为:Y>X>Z,故A错误;
B.X、Y、Z的最外层电子数分别为:1、7、3,则最外层电子数大小:Y>Z>X,故B正确;
C.X、Y、Z的原子序数分别为:11、17、13,则原子序数大小为:Y>Z>X,故C错误;
D.X、Y、Z的单质分别为金属钠、金属铝和氯气,铝的熔点最高,钠的熔点较低,氯气常温下为气体,所以其单质熔点大小为:Al>Na>Cl2,即:Y>Z>X,故D错误;
故选B.
点评 本题考查了位置、结构与性质关系的综合应用,题目难度中等,推断各元素名称为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,明确推断微粒半径大小常用方法.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
12.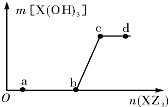 向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
 向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A. | d点对应的溶液中:K+、NH4+、CO32-、I- | |
| B. | c点对应的溶液中:Ag+、Ca2+、NO3-、Na+ | |
| C. | b点对应的溶液中:Na+、S2-、SO42-、Cl- | |
| D. | a点对应的溶液中:Na+、K+、SO42-、HCO3- |
13.溶液可能存在电离平衡、水解平衡和溶解平衡等动态平衡.下列说法中正确的是( )
| A. | 25℃时,HClO溶液加水稀释,电离程度增大,溶液中H+浓度增大 | |
| B. | 等物质的量浓度的氨水和盐酸等体积混合,存在:2c(NH4+)+c(H+)+c(NH3•H2O)=2c(Cl-)+c(OH-) | |
| C. | MgCl2饱和溶液蒸干可以得到MgCl2•6H2O,继续灼烧得到无水MgCl2 | |
| D. | 已知Ksp(AgCl)=1.8×10-10(mol/L)2,Ksp(Ag2CrO4)=1.8×10-10(mol/L)3,则Ag2CrO4的溶解度小于AgCl |
11.有机物A的分子式为C6H12O3,一定条件下,A与碳酸氢钠、钠均能产生气体,且生成的气体体积比(同温同压)为1:1,则A的结构最多有( )
| A. | 33种 | B. | 31种 | C. | 28种 | D. | 19种 |
18.下列有关苯酚钠溶液的叙述,正确的是( )
| A. | 该溶液呈碱性的原因是:C6H5O-+H2O=C6H5OH+OH- | |
| B. | 与少量CO2反应的离子方程式为:2C6H5O-+CO2+H2O=2C6H5OH+CO32- | |
| C. | 25℃时,该溶液中由水电离出的氢离子浓度大于1×10-7mol•L-1 | |
| D. | 该溶液中可能大量存在:K+、SO42-、Cl2、H+ |
8.下列关系正确的是( )
| A. | 含氢量:苯>乙烯>甲烷 | |
| B. | 密度:H2O>溴苯> | |
| C. | 沸点:戊烷>2-甲基丁烷>2,2-二甲基丙烷 | |
| D. | 等质量的下列物质燃烧耗O2量:乙炔>乙烯>乙烷 |
15.当光束通过下列分散系时,能产生丁达尔效应的是( )
| A. | 蔗糖溶液 | B. | 淀粉胶体 | C. | 氯化钠溶液 | D. | 氢氧化钠溶液 |
12.对下列化学用语描述和理解都正确的是( )
| A. | 原子结构示意图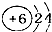 ,可以表示12C,也表示14C ,可以表示12C,也表示14C | |
| B. | 比例模型 可以表示水分子,也可以表示二氧化碳分子 可以表示水分子,也可以表示二氧化碳分子 | |
| C. | 结构示意图为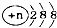 的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 | |
| D. | 电子式 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
13.天然油脂结构的核心为甘油[HOCH2CH(OH)CH2OH],有一瘦身用的非天然油脂,其结构的核心则为蔗糖(C12H22O11).该非天然油脂可由直链型的不饱和油酸(C17H33COOH)与蔗糖反应而得,其反应示意图如图所示(注意图中的反应式不完整).
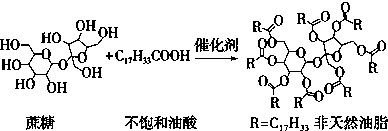
下列说法正确的是( )

下列说法正确的是( )
| A. | 蔗糖酯也是高级脂肪酸的甘油酯,属于油脂类物质 | |
| B. | 该非天然油脂与氢氧化钠溶液共热,其水解产物不与溴水反应 | |
| C. | 非天然油脂为高分子化合物 | |
| D. | 该蔗糖酯在稀硫酸的作用下水解,最终可生成多种有机分子 |