题目内容
8.在室温条件下,如下方法配制溶液,其浓度正确的是( )| A. | 1mol Na2CO3固体溶于1L水中配成溶液,其物质的量浓度为1mol/L | |
| B. | 40g NaOH固体溶于100g水,配成的溶液质量百分比浓度为40% | |
| C. | 22.4L氨气溶于水配成1L溶液,其物质的量浓度为1mol/L | |
| D. | 1mol NaCl固体溶于水配成1L溶液,其物质的量浓度为1mol/L |
分析 A.1mol Na2CO3固体溶于1L水中配成溶液,所得溶液体积不是1L;
B.溶质质量为40g,而溶液质量为140g,溶质质量分数小于40%;
C.没有告诉标况下,不能使用标况下的气体摩尔体积计算;
D.根据物质的量浓度c=$\frac{n}{V}$计算.
解答 解:A.1mol Na2CO3固体溶于1L水中配成溶液,配制的溶液体积不是1L,则物质的量浓度不是1mol/L,故A错误;
B.40g NaOH固体溶于100g水,溶液质量为140g,则溶液质量百分比浓度为:$\frac{40g}{140g}$×100%<40%,故B错误;
C.不是标况下,不能使用标况下的气体摩尔体积计算22.4L氨气的物质的量,故C错误;
D.1molaCl固体溶于水配成1L溶液,其物质的量浓度为:$\frac{1mol}{1L}$=1mol/L,故D正确;
故选D.
点评 本题考查了物质的量浓度的计算与判断,题目难度不大,明确物质的量浓度的概念及表达式即可解答,注意溶液体积V必须为最终配制溶液体积,不是加入的水的体积,C为易错点,需要明确标况下气体摩尔体积的使用条件.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
18.把a,b,c三块金属片浸入稀硫酸中,用导线两两相连组成原电池,若a,b相连时,a为负数;b,c相连时,电子由c经导线流向b;a,c相连时,c极上产生大量气泡,则三种金属的活动性由强到弱的顺序为( )
| A. | a>b>c | B. | a>c>b | C. | c>a>b | D. | c>b>a |
19.今有A、B两种原子,A原子的M层比B原子的M层少3个电子,B原子的L层电子数恰为A原子L层电子数的2倍,A和B分别是( )
| A. | Si和Na | B. | B和H | C. | Cl和C | D. | C和Al |
16.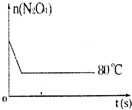 在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:N2O4?2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:N2O4?2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
(1)计算20s-40s内用N2O4表示的平均反应速率为0.002mol/(L•s).
(2)80℃该反应的平衡常数K=1.8mol•L-1.
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色变浅(填“变浅”、“变深”或“不变”).
(4)要增大该反应的K值,可采取的措施有(填序号)D,若要重新达到平衡时,使[NO2]/[N2O4]值变小,可采取的措施有(填序号)AB.
A.增大N2O4的起始浓度 B.向混合气体中通入NO2
C.使用高效催化剂 D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线.
 在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:N2O4?2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:N2O4?2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:| 时间(s)n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)80℃该反应的平衡常数K=1.8mol•L-1.
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色变浅(填“变浅”、“变深”或“不变”).
(4)要增大该反应的K值,可采取的措施有(填序号)D,若要重新达到平衡时,使[NO2]/[N2O4]值变小,可采取的措施有(填序号)AB.
A.增大N2O4的起始浓度 B.向混合气体中通入NO2
C.使用高效催化剂 D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线.
3.按如图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体是( )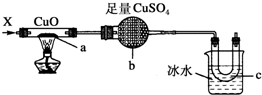

| A. | H2 | B. | CO和H2 | C. | NH3 | D. | CH3CH2OH(气) |
13.NA为阿伏加德罗常数,下列有关说法中正确的是( )
| A. | 2.3 g Na被O2完全氧化生成Na2O和Na2O2混合物时,失去电子数为0.1~0.2 NA | |
| B. | 常温下,64 g SO2所含的氧原子数为2NA | |
| C. | 标准状况下,等物质的量的SO2和SO3所占体积相同 | |
| D. | 100 mL 0.1 mol•L-1的硫酸铝溶液中含有的Al3+为0.02NA个 |
20.已知有机物甲、乙、丙有如下信息:
据此推断:
(1)甲的分子式为C3H8,若甲分子中有2个氢原子被F原子取代,所得的有机产物可能有4种.
(2)乙是性能优良的环保产物,可代替某些破坏臭氧层的氟利昂产品用作制冷剂.其分子中C、H、F的原子个数之比为1:2:2,则乙的结构式为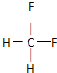 .下列关于乙的叙述正确的是D.
.下列关于乙的叙述正确的是D.
A.其分子构型为正四面体形 B.它能使溴水褪色
C.1mol 乙最多能与1mol F2 发生取代反应 D.它没有同分异构体
(3)将甲、乙按物质的量之比1:1混合,所得混合物的平均摩尔质量等于丙的摩尔质量,且丙分子不存在同分异构体,则丙的分子式为C2H5F.
| 甲 | 乙 | 丙 | |
| 所含元素 | C、H | C、H、F | C、H、F |
| 所含电子数 | 26 | ||
| 结构特点 | 饱和有机物 | ||
(1)甲的分子式为C3H8,若甲分子中有2个氢原子被F原子取代,所得的有机产物可能有4种.
(2)乙是性能优良的环保产物,可代替某些破坏臭氧层的氟利昂产品用作制冷剂.其分子中C、H、F的原子个数之比为1:2:2,则乙的结构式为
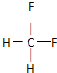 .下列关于乙的叙述正确的是D.
.下列关于乙的叙述正确的是D.A.其分子构型为正四面体形 B.它能使溴水褪色
C.1mol 乙最多能与1mol F2 发生取代反应 D.它没有同分异构体
(3)将甲、乙按物质的量之比1:1混合,所得混合物的平均摩尔质量等于丙的摩尔质量,且丙分子不存在同分异构体,则丙的分子式为C2H5F.