题目内容
相同温度下,在水中分别加入下列物质,若用KW表示水的离子积,α表示水的电离度,能使
的值增大的是( )
| α |
| KW |
| A、NaOH |
| B、NaHSO4 |
| C、NH4NO3 |
| D、KCl |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:酸和碱抑制水的电离,水解的盐促进水的电离,不水解的盐对水的电离无影响,KW只与温度有关,依此进行判断.
解答:
解:A.加入氢氧化钠,抑制水的电离,α减小,KW不变,故
减小,故A错误;
B.加入NaHSO4,电离出氢离子,抑制水的电离,α减小,KW不变,故
减小,故B错误;
C.加入NH4NO3,铵根离子发生水解,促进水的电离,α增大,KW不变,故
增大,故C正确;
D.加入KCl,对水的电离不产生影响,α不变,KW不变,故
不变,故D错误,
故选C.
| α |
| KW |
B.加入NaHSO4,电离出氢离子,抑制水的电离,α减小,KW不变,故
| α |
| KW |
C.加入NH4NO3,铵根离子发生水解,促进水的电离,α增大,KW不变,故
| α |
| KW |
D.加入KCl,对水的电离不产生影响,α不变,KW不变,故
| α |
| KW |
故选C.
点评:本题考查水的电离的影响因素,难度不大.要注意KW只与温度有关.

练习册系列答案
相关题目
下列有关Na2CO3和NaHCO3的性质的比较中,前者小于后者的是( )
| A、热稳定性 |
| B、常温时的溶解度 |
| C、常温时同浓度的pH |
| D、与含1mol HCl的盐酸完全反应时所需的物质的量 |
用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、一定条件下,1mol N2和3mol H2充分反应,生成物中的N-H键数目为6NA |
| B、1L 0.1mol?L-1的Na2S的溶液中S2-与HS-的总数为0.1NA |
| C、向含有FeI2的溶液中通入适量氯气,当有1mol Fe2+被氧化时,该反应转移电子的数目至少为3NA |
| D、1L 0.5mol?L-1 (NH4)2SO4溶液中NH4+数目为NA |
分别取等物质的量浓度的NaOH溶液各100mL,再通入一定量的CO2随后分别各取20mL溶液,向其中逐滴滴入0.2mol/L的盐酸,在标准状况下产生CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B两种情况):下列说法正确的是( )


| A、在A情况下,溶质是NaOH和Na2CO3的混合物,其物质的量之比为2:1 |
| B、在B情况下,溶质是Na2CO3和NaHCO3的混合物,其物质的量之比为1:2 |
| C、在B情况下,溶质只有Na2CO3 |
| D、原NaOH溶液的物质的量浓度为1.5 mol/L |
下列各组物质分别在空气中充分燃烧,产物完全相同的是( )
| A、H2和CO |
| B、C和CO |
| C、CO和CH4 |
| D、H2和C |
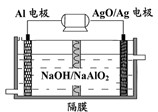 铝是日常生活中用途最多的金属元素,如图为Al-AgO电池的构造简图,电解质溶液为NaOH,它可用作水下动力电源,该电池中铝做
铝是日常生活中用途最多的金属元素,如图为Al-AgO电池的构造简图,电解质溶液为NaOH,它可用作水下动力电源,该电池中铝做