题目内容
浓度为0.1mol/L和1mol/L的盐酸分别与大理石(CaCO3)反应,谁快谁慢?为什么?
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:盐酸与大理石反应的实质为2H++CaCO3=Ca2++CO2↑+H2O,影响反应速率的主要因素是浓度、温度和固体表面积,以此解答.
解答:
解:0.1mol/L和1mol/L的盐酸浓度不同,浓度越大,反应速率越大,则1mol/L的盐酸反应速率较大.
答:1mol/L的盐酸;浓度越大,反应速率越大.
答:1mol/L的盐酸;浓度越大,反应速率越大.
点评:本题考查影响化学反应速率的因素,把握温度、浓度、接触面积影响反应速率即可解答,注意相关基础知识的积累,题目难度不大.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
下列与有机物的结构、性质有关的叙述正确的是( )
| A、乙烯和聚乙烯都可以与溴水发生加成反应 |
| B、醇与所有酸的反应都是酯化反应 |
| C、乙烷与氯气发生取代反应生成的有机物共有9种 |
| D、在有机物分子中,两个羟基去掉一分子水的反应就是酯化反应 |
下列属于化学性质的是 ( )
| A、溶解性 | B、挥发性 |
| C、金属活动性 | D、导电性 |
相同温度下,在水中分别加入下列物质,若用KW表示水的离子积,α表示水的电离度,能使
的值增大的是( )
| α |
| KW |
| A、NaOH |
| B、NaHSO4 |
| C、NH4NO3 |
| D、KCl |
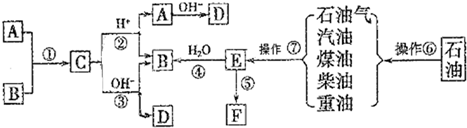
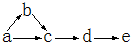 a、b、c、d、e是含有一种相同元素的五种物质,可发生如右图所示的转化.其中:a是单质;c、d是氧化物;e是最高价氧化物对应的水化物.
a、b、c、d、e是含有一种相同元素的五种物质,可发生如右图所示的转化.其中:a是单质;c、d是氧化物;e是最高价氧化物对应的水化物.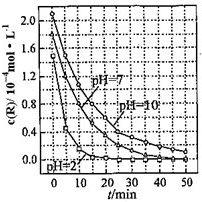 一定条件下,溶液的酸碱性对TiO2光催化燃料R降解反应的影响如图所示.请回答下列问题:
一定条件下,溶液的酸碱性对TiO2光催化燃料R降解反应的影响如图所示.请回答下列问题: