题目内容
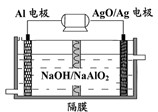 铝是日常生活中用途最多的金属元素,如图为Al-AgO电池的构造简图,电解质溶液为NaOH,它可用作水下动力电源,该电池中铝做
铝是日常生活中用途最多的金属元素,如图为Al-AgO电池的构造简图,电解质溶液为NaOH,它可用作水下动力电源,该电池中铝做考点:原电池和电解池的工作原理
专题:电化学专题
分析:该装置是原电池,铝作负极,电极反应为Al-3e-+4OH-═AlO2-+2H2O,AgO为正极,正极上的电极反应式为AgO+2e-+H2O═Ag+2OH-,以此解答该题.
解答:
解:由装置图可知,Al被氧化生成AlO2-,应为电池的负极,电极反应为Al-3e-+4OH-=AlO2-+2H2O,
故答案为:负;Al-3e-+4OH-=AlO2-+2H2O.
故答案为:负;Al-3e-+4OH-=AlO2-+2H2O.
点评:本题考查化学电源新型电池,题目难度中等,解答本题的关键是能正确书写电极方程式,做题时注意体会书写方法.

练习册系列答案
相关题目
相同温度下,在水中分别加入下列物质,若用KW表示水的离子积,α表示水的电离度,能使
的值增大的是( )
| α |
| KW |
| A、NaOH |
| B、NaHSO4 |
| C、NH4NO3 |
| D、KCl |
如图是一些常见有机物的转化关系,以下有关反应的说法不正确的是( )
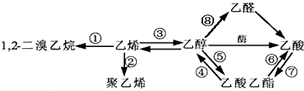

| A、反应①是加成反应 |
| B、反应②是加聚反应 |
| C、反应③是消去反应 |
| D、反应④⑤⑥是取代反应 |
在实验室中,下列除去杂质的方法正确的是( )
| A、溴苯中混有溴,加入KI溶液,振荡,再用汽油萃取 |
| B、硝基苯中混有浓硝酸和浓硫酸,将其倒入到NaOH溶液中,静置,分液 |
| C、乙烷中混有乙烯,通氢气在一定条件下反应,使乙烯转化为乙烷 |
| D、乙烯中混有SO2和CO2,将其先后通入NaOH和KMnO4溶液中洗气 |
光具有能量,能影响很多反应.下列反应中,受光照影响显著的是( )
| A、乙醇与乙酸的酯化反应 |
| B、甲烷与氧气的反应 |
| C、铁与氯气的反应 |
| D、次氯酸的分解 |