题目内容
19.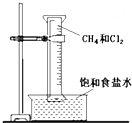 如图所示,用排饱和食盐水法先后收集20ml CH4和 80mlCl2,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸),等待片刻,观察发生的现象.回答下列问题:
如图所示,用排饱和食盐水法先后收集20ml CH4和 80mlCl2,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸),等待片刻,观察发生的现象.回答下列问题:(1)大约30min后,可以观察到量筒壁上出现油状液体,该现象说明生成了②③④(填序号)
①CH3Cl; ②CH2 Cl2;③CHCl3; ④CCl4
量筒内出现的白雾是盐酸的小液滴,量筒内液面上升(填“上升”、“下降”或“不变”),
(2)液化石油气的主要成分是丙烷,试写出丙烷燃烧的化学方程式C3H8+5O2点燃→3CO2+4H20.将现用液化石油气的燃具改用天然气时应减少进空气的风口.(填增大或减少)
(3)下列烷烃的分子式有 3种同分异构体的是A.(填字母)
A.C5H12; B.C4H10; C.C3H8; D.C2H6.
分析 (1)二氯甲烷、三氯甲烷、四氯化碳均是油状的液体,的氯化氢极易溶于水,遇水蒸气形成白雾,容器中的压强较低,液面上升;
(2)丙烷燃烧生成二氧化碳和水;
(3)烷烃同分异构体书写技巧:先写最长链;然后从最长链减少一个碳原子作为取代基,在剩余的碳链上连接,即主链由长到短,支链由整到散,位置由中心排向两边.
解答 解:(1)甲烷可以和氯气发生取代反应,生成的二氯甲烷、三氯甲烷、四氯化碳均是油状的液体,一氯甲烷是气体,生成的氯化氢极易溶于水,遇水蒸气形成白雾,容器中的压强较低,液面上升,故答案为:油状;②③④;盐酸的小液滴;上升;
(2)丙烷和甲烷燃烧均生成二氧化碳和水:C3H8+5O2点燃→3CO2+4H20,CH4+2O2点燃→CO2+2H20,由反应可知,同物质的量即同体积的丙烷和甲烷,丙烷耗氧量多,故把液化石油气的灶具改用天然气为燃料时,需要减少空气气的量,
故答案为:C3H8+5O2点燃→3CO2+4H20;减少;
(3)C5H123种同分异构体;C4H102种同分异构体;C3H8、C2H6无同分异构体,故选A.
点评 本题考查甲烷与氯气的燃烧、同分异构体书写,难度较小,旨在考查学生对基础知识的理解与掌握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列各组中的分子,全部是以极性键形成的分子是( )
| A. | H2、N2、CCl4 | B. | CH4、NH3、H2O | C. | CO2、CS2、Cl2 | D. | HCl、NO、Br2 |
14.下列物质属于离子化合物是( )
| A. | SO2 | B. | H2O | C. | HCl | D. | NaOH |
11.下列分子属于手性分子的是( )
| A. | H2O | B. |  | C. |  | D. | H2N-CH2-COOH |
9.在某容积可变的密闭容器中,有下列的可逆反应:A(g)+B(g)?xC(g),有图1(T表示温度,P表示压强,C%表示C的体积分数)所示的反应曲线.试判断对图2的说法中正确的是( )

| A. | P3=P4,y轴表示C的体积分数 | |
| B. | P3<P4,y轴表示B的质量分数 | |
| C. | P3<P4,y轴表示混合气体的密度 | |
| D. | P3>P4,y轴表示混合气体的平均摩尔质量 |
 某校化学兴趣小组为探究FeSO4和NaHCO3的反应,按如图所示操作将NaHCO3溶液滴加到FeSO4溶液中(FeSO4和NaHCO3溶液均用经煮沸后冷却的蒸馏水配制,并在FeSO4溶液中加入少量铁粉).观察到试管中立即出现白色沉淀,同时有大量无色气体生成.
某校化学兴趣小组为探究FeSO4和NaHCO3的反应,按如图所示操作将NaHCO3溶液滴加到FeSO4溶液中(FeSO4和NaHCO3溶液均用经煮沸后冷却的蒸馏水配制,并在FeSO4溶液中加入少量铁粉).观察到试管中立即出现白色沉淀,同时有大量无色气体生成. .
.
 .
. .
. 分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计.请回答下列问题:
分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计.请回答下列问题:
 ;F
;F
 +O2
+O2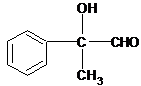 +2H2O
+2H2O +Cu2O↓+2H2O
+Cu2O↓+2H2O .
.