题目内容
2.有人设计了以下反应途径制H2,假设反应都能进行,你认为最合理的是( )| A. | C3H8$\stackrel{极高温}{→}$3C+4H2 | |
| B. | C3H8$\stackrel{高温脱氢}{→}$C3H6+H2 | |
| C. | C3H8+3H2O$\stackrel{催化剂}{→}$3CO+7H2 | |
| D. | C3H8+5O2→3CO2+4H2O,2H2O$\stackrel{电解}{→}$2H2↑+O2↑ |
分析 在工业生产中应考虑经济效益,反应机理要低成本、低能耗,从所给的几种反应途径来看,A、耗能高、原料利用率低,D会消耗电能,也比较麻烦,而BC选项能耗低、原料利用率高,相同物质的量的丙烷C选项产生的H2较多,据此即可解答.
解答 解:在工业生产中应考虑经济效益,反应机理要低成本、低能耗.所以从经济效益的角度考虑,“极高温”和“通电”都需要有较大的经济投入,A、B、D不选;
C反应能耗小且产生氢气多故最合理,故选:C.
点评 本题考查了物质的制备和转化,通过对多种方案分析比较,结合物质的性质寻找合适的方案是解答的关键,题目难度较小.

练习册系列答案
相关题目
12.NA为阿伏伽德罗常数.下列说法正确的是( )
| A. | 同温同压同体积的CO2和SO2所含氧原子数均为2NA | |
| B. | 32g Cu与足量的S完全反应转移的电子数为NA | |
| C. | 标况下,11.2L乙烷中含有共价键的数目为3.5NA | |
| D. | 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA |
13.下列关于油脂的叙述不正确的是( )
| A. | 油脂在一定条件下能发生皂化反应 | B. | 油脂属于酯类 | ||
| C. | 油脂无固定的熔沸点 | D. | 油脂都不能使溴水褪色 |
10.家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中发生的化学反应是( )
①4Fe(OH)2+2H2O+O2═4Fe(OH)3 ②2Fe2++2H2O+O2+4e-═2Fe(OH)2
③2H2O+O2+4e-═4OH- ④Fe-3e-═Fe3+.
①4Fe(OH)2+2H2O+O2═4Fe(OH)3 ②2Fe2++2H2O+O2+4e-═2Fe(OH)2
③2H2O+O2+4e-═4OH- ④Fe-3e-═Fe3+.
| A. | ①② | B. | ③④ | C. | ①③ | D. | ①②③④ |
17.已知c(NH4Cl)<0.1moL/L时,溶液的pH>5.1,现用0.1mol/L盐酸滴定10mL0.05mol/L氨水,用甲基橙作指示剂,达到终点时所用盐酸的量应是( )
| A. | 10 mL | B. | 5 mL | C. | 大于5mL | D. | 小于5mL |
7.能用来检测酒精中是否有水的试剂是( )
| A. | 浓硫酸 | B. | 钠 | C. | 碱石灰 | D. | 无水硫酸铜 |
14.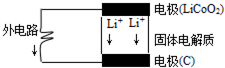 苹果iphone6正在我国热卖,其电池为锂电池.构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
苹果iphone6正在我国热卖,其电池为锂电池.构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
 苹果iphone6正在我国热卖,其电池为锂电池.构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
苹果iphone6正在我国热卖,其电池为锂电池.构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )| A. | 该电池放电时的负极材料为LiCoO2 | |
| B. | 电池中的固体电解质可以是熔融的氯化钠、氯化铝等 | |
| C. | 充电时的阴极反应:Li1-xCoO2+xLi++xe-═LiCoO2 | |
| D. | 外电路上的“→”表示放电时的电子流向 |
12.下列说法正确的是( )
| A. | 3.0g C2H6中含有共用电子对的数目为0.7×6.02×1023 | |
| B. | 25℃时pH=1的醋酸溶液中含有H+的数目为0.1×6.02×1023 | |
| C. | 已知2CO(g)+O2(g)?2CO2(g)△H=-a kg•mol-1,将2NA个CO与NA个O2混合,充分反应放出a kJ的热量 | |
| D. | 50mL 18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
