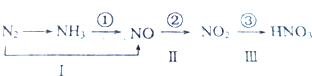题目内容
2.已知0.1mol•L-1邻苯二甲酸(二元酸)溶液的pH大于1,取等体积的邻苯二甲酸溶液和某KOH溶液混合,测得混合液的pH等于7,则碱与酸的浓度比值(X)为( )| A. | X>2 | B. | X=2 | C. | 2>X>1 | D. | X=1 |
分析 0.1mol•L-1邻苯二甲酸(二元酸)溶液的pH大于1,则邻苯二甲酸为二元弱酸;当碱与酸的浓度比值(X)为2时,反应生成强碱弱酸盐邻苯二甲酸钠,溶液显示碱性;当碱与酸的浓度比值(X)为1时,邻苯二甲酸中羧基剩余,溶液显示酸性,若满足反应后溶液为中性,则1<X<2.
解答 解:已知0.1mol•L-1邻苯二甲酸(二元酸)溶液的pH大于1,说明邻苯二甲酸为二元弱酸,
当碱与酸的浓度比值X=2时,反应生成强碱弱酸盐邻苯二甲酸钠,由于邻苯二甲酸钠部分水解,溶液显示碱性;
当碱与酸的浓度比值X=1时,邻苯二甲酸中羧基剩余一半,电离程度大于水解程度,溶液显示酸性,
若等体积的两溶液混合,使反应后溶液为中性,则一定满足:1<X<2,
故选C.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,根据题中信息明确邻苯二甲酸为二元弱酸为解答关键,注意明确溶液酸碱性与溶液pH的关系及计算方法.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
13.以硼镁矿( 2MgO.B2O3.H2O、SiO2及少量Fe3O4、CaCO3、Al2O3 )为原料生产硼酸的工艺流程如下:

已知:表一:不同温度下H3BO3的溶解度
表二:不同物质沉淀完全时的pH
(1)由于矿粉中含CaCO3,“浸取”时容易产生大量泡沫使物料从反应器中溢出,应采取的措施为应分批加入H2SO4 .
(2)“浸出液”显酸性,含有H3BO3、Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质.“除杂”时,向浸出液中依次加入适量目H2O2和MgO,可以除去的杂质离子为Fe3+、Fe2+、Al3+,的作用为H2O2+2H++2Fe2+=2Fe3++2H2O(用离子方程式表示).
(3)“浸取”后,采用“热过滤”的目的为防止温度下降时H3BO3从溶液中析出.
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图所示,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收 MgSO4.H2O,应采取的措施是将“母液”蒸发浓缩,加压升温结晶.

(5)已知25℃时,硼酸( H3BO3)溶液中存在如下平衡:HBO3(aq)+H2O(l)?[B(OH)4]-(aq)+H+(aq) K=5.7×10-10;25℃时,0.7mol.L-1硼酸溶液中c(H)+≈2×10-5mol.L-1
(6)已知25℃时:
下列说法正确的是BD(填选项字母).
A.碳酸钠溶液滴入硼酸溶液中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸溶液中能观察到有气泡产生
C.等浓度碳酸溶液和硼酸溶液的pH:前者>后者
D.等浓度碳酸钠溶液和醋酸钠溶液的pH:前者>后者.

已知:表一:不同温度下H3BO3的溶解度
| 温度℃) | 20 | 40 | 60 | 100 |
| 溶解度(g) | 5.0 | 8.7 | 14.8 | 40.2 |
| 物质 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| pH | 3.2 | 5.2 | 9.7 | 12.4 |
(2)“浸出液”显酸性,含有H3BO3、Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质.“除杂”时,向浸出液中依次加入适量目H2O2和MgO,可以除去的杂质离子为Fe3+、Fe2+、Al3+,的作用为H2O2+2H++2Fe2+=2Fe3++2H2O(用离子方程式表示).
(3)“浸取”后,采用“热过滤”的目的为防止温度下降时H3BO3从溶液中析出.
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图所示,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收 MgSO4.H2O,应采取的措施是将“母液”蒸发浓缩,加压升温结晶.

(5)已知25℃时,硼酸( H3BO3)溶液中存在如下平衡:HBO3(aq)+H2O(l)?[B(OH)4]-(aq)+H+(aq) K=5.7×10-10;25℃时,0.7mol.L-1硼酸溶液中c(H)+≈2×10-5mol.L-1
(6)已知25℃时:
| 化学式 | H2CO3 | CH3COOH |
| 电离常数 | K1=4.4×10-7 K2=4.7×10-11 | K=1.75×10-5 |
A.碳酸钠溶液滴入硼酸溶液中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸溶液中能观察到有气泡产生
C.等浓度碳酸溶液和硼酸溶液的pH:前者>后者
D.等浓度碳酸钠溶液和醋酸钠溶液的pH:前者>后者.
7.相同条件下,用下列物质做氧化剂收集相同Cl2消耗浓盐酸最多的是( )
| A. | MnO2 | B. | KMnO4 | C. | NaClO | D. | KClO3 |
14.用沉淀法测定NaHCO3和K2CO3混合物的组成.实验过程是每次称取一定质量的样品溶于水制成溶液,向其中滴加相同浓度的Ba(OH)2溶液,每次实验均充分反应.实验记录见下表:
回答下列问题:
(1)写出少量NaHCO3和过量Ba(OH)2溶液反应的离子方程式Ba2++HCO3-+OH-═BaCO3↓+H2O.
(2)第2次实验中产生沉淀的质量是2.758g.
(3)样品中NaHCO3和K2CO3的物质的量之比是2:5.
(4)原Ba(OH)2溶液的浓度为0.056mol•L-1.
(5)室温下取第3组实验所得溶液的1/10,加水配成500mL溶液,则稀释以后溶液的pH值为12.
| 实验次数 | 称取样品的质量/g | 所加Ba(OH)2溶液的体积/mL | 测得生成沉淀的质量/g |
| 1 | 0.858 | 500 | 1.379 |
| 2 | 1.716 | 500 | |
| 3 | 2.574 | 500 | 4.137 |
| 4 | 3.432 | 500 | 5.516 |
| 5 | 4.290 | 500 | 5.516 |
| 6 | 5.148 | 500 | 5.516 |
(1)写出少量NaHCO3和过量Ba(OH)2溶液反应的离子方程式Ba2++HCO3-+OH-═BaCO3↓+H2O.
(2)第2次实验中产生沉淀的质量是2.758g.
(3)样品中NaHCO3和K2CO3的物质的量之比是2:5.
(4)原Ba(OH)2溶液的浓度为0.056mol•L-1.
(5)室温下取第3组实验所得溶液的1/10,加水配成500mL溶液,则稀释以后溶液的pH值为12.
16.室温下,某研究小组为探究影响CaCO3与盐酸反应速率的因素,进行了如下实验.
(1)测定0.5mol•L-1盐酸与CaCO3固体的反应速率.
方案1:通过测定生成CO2的体积(或质量)和反应时间计算反应速率;
方案2:通过测定消耗CaCO3固体的质量和反应时间计算反应速率;
(2)探究固体表面积或反应物浓度对化学反应速率的影响.限选试剂与用品:0.5mol•L-1盐酸、块状CaCO3、粉末状CaCO3、蒸馏水、量筒、秒表
①设计实验:在固体表面积或反应物浓度不同的条件下,通过如图1实验装置测定生成等质量CO2所需的时间(或相同时间内生成的CO2的质量)来直接体现反应速率大小.

②参照下表格式,拟定实验表格,完整体现实验方案(写出所选试剂的状态及体积,需测定的物理量数据可用字母表示).
(3)实验结束后,研究小组将0.1mol•L-1Na2CO3溶液缓慢滴加至实验1反应后的混合溶液中,研究产生沉淀的量,请在图2中画出产生沉淀的质量与滴加Na2CO3溶液体积之间关系的示意图.
(1)测定0.5mol•L-1盐酸与CaCO3固体的反应速率.
方案1:通过测定生成CO2的体积(或质量)和反应时间计算反应速率;
方案2:通过测定消耗CaCO3固体的质量和反应时间计算反应速率;
(2)探究固体表面积或反应物浓度对化学反应速率的影响.限选试剂与用品:0.5mol•L-1盐酸、块状CaCO3、粉末状CaCO3、蒸馏水、量筒、秒表
①设计实验:在固体表面积或反应物浓度不同的条件下,通过如图1实验装置测定生成等质量CO2所需的时间(或相同时间内生成的CO2的质量)来直接体现反应速率大小.

②参照下表格式,拟定实验表格,完整体现实验方案(写出所选试剂的状态及体积,需测定的物理量数据可用字母表示).
 | V(0.5mol•L-1 HCl)/mL | m(CaCO3)/g | CaCO3状态 | V(蒸馏水)/mL | 实验目的 | |
| 实验1 | 40.0 | 0.8 | ①实验1和2探究固体表面积对反应速率的影响; ②实验1和3探究反应物浓度对反应速率的影响 | |||
| 实验2 | 40.0 | 0.8 | ||||
| 实验3 | 60.0 | 0.8 |
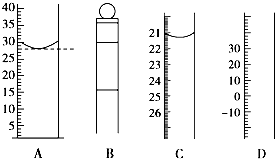 (1)图为常见仪器的部分结构(有的仪器被放大)
(1)图为常见仪器的部分结构(有的仪器被放大)