题目内容
17.在一10L的密闭容器中充入SO2和O2发生反应:2SO2(g)+O2(g)?2SO3(g),测得4min内O2的物质的量由开始的18mol降到14mol,再过tminO2的物质的量变为10mol.求:(1)4min求SO3的浓度;
(2)4min内用SO2表示的反应速率;
(3)t>(填“<”“>”或“=”)4min,理由是随反应进行物质浓度减小,反应速率减小,达到平衡的时间长.
分析 测得4min内O2的物质的量由开始的18mol降到14mol,反应的氧气为18mol-14mol=4mol,
(1)物质浓度c=$\frac{n}{V}$;
(2)反应速率v=$\frac{△c}{△t}$计算得到;
(3)再过tminO2的物质的量变为10mol,尽管减少的物质的量相同,但随反应进行物质浓度减小,反应速率减小.
解答 解:在一10L的密闭容器中充入SO2和O2发生反应:2SO2(g)+O2(g)?2SO3(g),测得4min内O2的物质的量由开始的18mol降到14mol,反应的氧气为18mol-14mol=4mol,
2SO2(g)+O2(g)?2SO3(g)
变化量 8 4 8
(1)4min求SO3的浓度=$\frac{8mol}{10L}$=0.8mol/L,答:4min求SO3的浓度为0.8mol/L;
(2)4min内用SO2表示的反应速率=$\frac{\frac{8mol}{10L}}{4min}$=0.2mol/(L•min),答:4min内用SO2表示的反应速率0.2mol/(L•min);
(3)测得4min内O2的物质的量由开始的18mol降到14mol,再过tminO2的物质的量变为10mol,反应过程中消耗氧气物质的量都是4mol,但随反应进行反应物的浓度减小,反应速率减小,达到平衡所需时间长,
故答案为:>;随反应进行反应物的浓度减小,反应速率减小,达到平衡所需时间长.
点评 本题考查了化学反应后物质浓度、速率的计算分析应用,主要是一些反应速率因素的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.部分弱酸的电离平衡常数如下表:
下列选项正确的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.3×10-7,K2=5.6×10-11 |
| A. | 在NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-) | |
| B. | 向NaCN溶液中通入少量CO2的离子方程式:2CN-+H2O+CO2=2HCN+CO32- | |
| C. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者 | |
| D. | 等物质的量浓度的各溶液pH关系为:pH(NaHCO3)>pH(NaCN)>pH(HCOONa) |
8.己知某温度下,Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1.12×10-12,下列叙述正确的是( )
| A. | 向氯化银的浊液中加入氯化钠溶液,氯化银的溶解度减小 | |
| B. | 向2.0×10-1mol/L的K2CrO4溶液中加入等体积的2.0×10-1mol/LAgNO3溶液,则有Ag2CrO4沉淀生成 | |
| C. | 将一定量的AgCl和Ag2CrO4固体棍合物溶于蒸馏水中,充分溶解后,静置,上层清液中Cl-的物质的量浓度最大 | |
| D. | 将0.001 mol/L的AgNO3溶液滴入0.001mol/L的KCl和0.001 mol/L的K2CrO4溶液,则先产生AgCl沉淀 |
5.反应2A(g)+5B(g)?4C(g)+6D(g)在1L密闭容器中进行,0.5min后,A减少了0.90mol,则此反应的速率可表示为( )
| A. | v(A)=3.6mol/(L•s) | B. | v(B)=0.075mol/(L•s) | C. | v(C)=0.030mol/(L•s) | D. | v(D)=0.060mol/(L•s) |
12.在锌铜原电池中,当导线中有1mole-通过时,从理论上分析,两极的变化是( )
①锌片溶解了32.5g ②锌片增重了32.5g
③铜片上析出1g氢气 ④铜片上析出1mol氢气.
①锌片溶解了32.5g ②锌片增重了32.5g
③铜片上析出1g氢气 ④铜片上析出1mol氢气.
| A. | ①和③ | B. | ①和④ | C. | ②和③ | D. | ②和④ |
2.已知0.1mol•L-1邻苯二甲酸(二元酸)溶液的pH大于1,取等体积的邻苯二甲酸溶液和某KOH溶液混合,测得混合液的pH等于7,则碱与酸的浓度比值(X)为( )
| A. | X>2 | B. | X=2 | C. | 2>X>1 | D. | X=1 |
9.将某溶液逐滴加入Al(OH)3溶胶内,开始产生沉淀,继续滴加时沉淀又溶解,该溶液是( )
| A. | 2 mol/L NaOH的溶液 | B. | 2 mol/L Na2SO4的溶液 | ||
| C. | 2 mol/L MgSO4的溶液 | D. | FeCl3溶液 |
6.现在含MgCl2、AlCl3均为n mol的混合溶液,向其中滴NaOH溶液至过量.加入NaOH溶液的物质的量与生成沉淀的物质的量的关系正确的是(离子形成沉淀或沉淀的溶解与溶液pH的关系如下表)
( )
| 离子 | Mg2+ | Al3+ | 物质 | Al(OH)3 |
| 开始沉淀时的pH | 8.93 | 3.56 | 开始溶解时的pH | 8.04 |
| 完全沉淀时的pH | 10.92 | 4.89 | 完全溶解时的pH | 12.04 |
| A. | 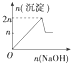 | B. |  | C. |  | D. |  |
