题目内容
6.设NA为阿伏加德罗常数的值.下列说法一定正确的是( )| A. | 将含0.1molFeCl3的溶液滴加到沸水中完全水解可生成0.1NA个Fe(OH)3胶粒 | |
| B. | 常温常压下,0.1molD216O中含中子数、质子数、电子数均为NA | |
| C. | 将0.1molCl2通入1L水中,转移的电子数为0.1NA | |
| D. | 电解饱和食盐水,当阴极产生1.12LH2时,转移的电子数一定为0.1NA |
分析 A.氢氧化铁胶粒为氢氧化铁的聚集体,无法计算氢氧化铁胶粒数目;
B.D216O分子中含中子数、质子数、电子数均为都是10;
C.氯气与水的反应中,只有部分氯气与水反应生成氯化氢和次氯酸;
D.没有告诉在标况下,不能使用标况下的气体摩尔体积计算.
解答 解:A.由于氢氧化铁胶粒为氢氧化铁的聚集体,则无法计算氢氧化铁胶体中含有的胶粒数目,故A错误;
B.D216O分子中含中子数、质子数、电子数均为都是10,则0.1molD216O中含中子数、质子数、电子数均为1mol,粒子数均为NA,故B正确;
C.将0.1molCl2通入1L水中,由于只有部分氯气与水反应,则反应转移的电子小于0.1mol,转移的电子数小于0.1NA,故C错误;
D.不是标况下,不能使用标况下的气体摩尔体积计算1.12L氢气的物质的量,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的应用,题目难度中等,注意明确标况下气体摩尔体积的使用条件,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
4.已知某酸H2B在水溶液中存在下列关系::①H2B?H++HB-,②HB-?H++B2-.则下列关于酸式盐NaHB的溶液
的说法中一定正确的是( )
的说法中一定正确的是( )
| A. | NaHB的电离方程式为:NaHB?Na-+H-+B2- | |
| B. | NaHB溶液一定呈酸性 | |
| C. | NaHB和NaOH溶液反应的离子方程式为H++OH-═H20 | |
| D. | NaHB溶液中一定存在:c(Na+)+c(H+)═c(HB-)+2c(B2-)+c(OH-) |
11.NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温下,78g Na202中含有的阴离子数为2NA | |
| B. | 常温下,1L 0.1 mol/L NH4NO3溶液中含有的NH4 +数为0.1NA | |
| C. | 标准状况下,22.4 L己烷中含有的共价键的数目为19 NA | |
| D. | 30 g SiO2晶体中含有Si-O键的数目为2 Na |
16.下列事实能说明某物质是强电解质的是( )
| A. | 该物质在水中的溶解度大 | |
| B. | 该物质的水溶液导电能力强 | |
| C. | 该物质的水溶液中不存在溶质分子 | |
| D. | 该物质的水溶液中不存在除水外的电离平衡 |
 ,结构简式H2C=CH2.
,结构简式H2C=CH2.
 ,反应类型是加聚反应.
,反应类型是加聚反应.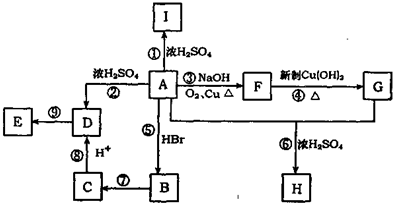
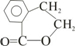 ;
;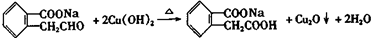 ;写出反应⑦的化学方程式
;写出反应⑦的化学方程式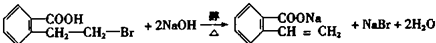 ;
;