题目内容
下图中,表示正反应是吸热反应的是( )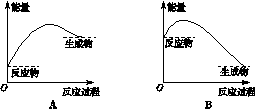
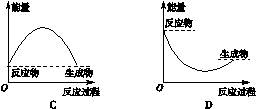
A
解析试题分析:如果反应物的总能量高于生成物的总能量,则该反应就是放热反应,反之是吸热反应。A中反应物的总能量低于生成物的总能量,反应是吸热反应;B中反应物的总能量高于生成物的总能量,反应是放热反应;C中反应物和生成物的总能量相等,不符合客观事实。D中反应物的总能量高于生成物的总能量,但反应的过程不正确,答案选A。
考点:考查放热反应和吸热反应的判断
点评:该题是基础性试题的考查,主要是考查学生对反应热含义以及放热反应和吸热反应判断的熟悉了解程度,有利于调动学生的学习兴趣,提高学生的学习效率。该题的关键是明确反应物和生成物总能量的相对大小与放热反应以及吸热反应的关系。

练习册系列答案
相关题目
下列图示与对应的叙述相符的是
| A.图I表示某放热反应在无催化剂(a)和有催化剂(b)时反应的能量变化 |
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3各成分的物质的量变化,t2时刻改变的条件可能是增加了SO2 2SO3各成分的物质的量变化,t2时刻改变的条件可能是增加了SO2 |
| C.图Ⅲ表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mLBa(OH)2溶液时铝离子恰好沉淀完全 |
| D.电导率可表示溶液导电性的强弱,电导率越大导电性越强。图Ⅳ可表示向盐酸和醋酸混合溶液中滴入氨水过程中电导率的变化关系 |
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如下图所示,下列结论不正确的是 ( )
| A.反应开始2 min内平均反应速率最大 |
| B.反应速率先增大后又减小 |
| C.反应开始4 min内温度对反应速率的影响比浓度大 |
| D.反应在第2 min到第4 min间生成CO2的平均反应速率为 v (CO2)="0.1" mol·min-1 |
36g碳不完全燃烧所得气体中,CO占三分之一体积,CO2占三分之二体积。已知:2C(s)+O2(g)=2CO(g)△H=-110.5kJ/mol,2CO(g)+O2(g) =2CO2(g)△H=-566kJ/mol,与这些碳完全燃烧相比,损失的热量是( )
| A.172.5kJ | B.1149kJ | C.517.5kJ | D.283kJ |
碘与氢气反应的热化学方程式是
①I2(g) + H2(g)  2HI(g) ΔH =-9.48 kJ·mol-1
2HI(g) ΔH =-9.48 kJ·mol-1
②I2(s) + H2(g)  2HI(g) ΔH =" +26.48" kJ·mol-1
2HI(g) ΔH =" +26.48" kJ·mol-1
下列说法正确的是( )
| A.①的产物比②的产物稳定 |
| B.I2(s) = I2(g) ΔH=" +17.00" kJ·mol-1 |
| C.②的反应物总能量比①的反应物总能量低 |
| D.1mol I2(g)中通入1 mol H2(g),发生反应时放热9.48 kJ |
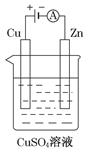

 溶液和氢气的总能量 (填“大于”“小于”或“等于”)镁片和稀盐酸的总能量。
溶液和氢气的总能量 (填“大于”“小于”或“等于”)镁片和稀盐酸的总能量。 H2(g)+CO2(g) ΔH=-41kJ·mol-1
H2(g)+CO2(g) ΔH=-41kJ·mol-1 
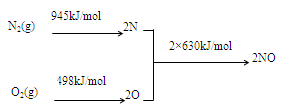
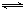 2NO(g) △H= 。
2NO(g) △H= 。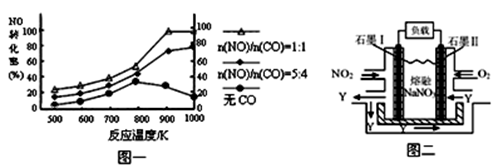
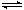 CH3OH(g)+H2O(g) ΔH<0合成甲醇。
CH3OH(g)+H2O(g) ΔH<0合成甲醇。