题目内容
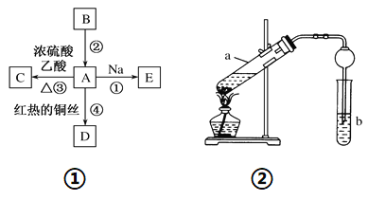
【题目】稀土有工业“黄金”之称,我国稀土资源丰富。目前从氟碳铈矿(主要化学成分为CeFCO3)提取铈族稀土元素的冶炼处理工艺已经发展到十几种,其中一种提取铈的工艺流程如下:

已知:①焙烧后烧渣中含+4价的铈及+3价的其它稀土氟氧化物:
②Ce4+能与SO42-结合成CeSO4,Ce4+能被萃取剂[(HA)2]萃取。
请回答下列问题:
(1)CeFCO3中,Ce元素的化合价为_____。
(2)“酸浸I”过程中CeO2转化为Ce3+,且产生黄绿色气体,用稀硫酸和H2O2,替换HCl就不会造成环境污染。则稀硫酸.H2O2与CeO2反应的离子方程式为:__________。
(3)“沉淀”步骤中发生的反应为:Ce(BF4)3(s)+3KCl(aq)=3KBF4(s)+CeCl3(aq)。已知Ce(BF4)3、KBF4的Ksp分别为a、b,则该反应的平衡常数为______(用含a、b的代数式表示)。
(4)“浸出液”中含有少量Ce4+及其他稀土元素的离子,可以通过“萃取”与“反萃取寻探作进一步分离、富集各离子。“萃取”时Ce4+与萃取剂[(HA)2]存在的反应为:Ce4++n(HA)2![]() Ce(H2a-4A2a)+4H+。用D表示Ce4+分别在有机层中与水层中存在形式的浓度之比(D=
Ce(H2a-4A2a)+4H+。用D表示Ce4+分别在有机层中与水层中存在形式的浓度之比(D=![]() )其它条件不变,在浸出液中加入不同量的NaSO4以改变水层中的c(SO42-),D随浸出液中c(SO42-)增大而减小的原因是__________。
)其它条件不变,在浸出液中加入不同量的NaSO4以改变水层中的c(SO42-),D随浸出液中c(SO42-)增大而减小的原因是__________。
(5)“操作I”后,向溶液中加入NaOH溶液,调节溶液的pH可获得Ce(OH)3沉淀,当溶液中离子浓度小于1.0×10-6mol/L视为沉淀完全,常温下加入NaOH调节溶液的pH应大于_______[已知:Ce(OH)3的Ksp=8.0×10-21;1g2=-0.3]
(6)写出“氧化”步骤的化学方程式:_______________。
(7)CeO2是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧在尾气消除过程中发生着CeO2![]() CeO2(1-x) +xO2↑(0≤x≤0.25)的循环。写出CeO2消除CO尾气的化学方程式:________________。
CeO2(1-x) +xO2↑(0≤x≤0.25)的循环。写出CeO2消除CO尾气的化学方程式:________________。
【答案】 +3(或+3价) 2CeO2+H2O2+6H+=2Ce3++4H2O+O2↑ a/b3 随着c(SO42-)增大,水层中Ce4+被SO42-结合成[CeSO4]2+,c([CeSO4]2+)增大,同时导致Ce4++n(HA)2 ![]() Ce(H2n-4A2n)+4H+向左(逆向)移动,致使c[Ce(H2n-4A2n)]减小 9.3 2Ce(OH)3+NaClO+H2O=2Ce(OH)4+NaCl 2xCO+CeO2=CeO2(1-x)+2xCO2
Ce(H2n-4A2n)+4H+向左(逆向)移动,致使c[Ce(H2n-4A2n)]减小 9.3 2Ce(OH)3+NaClO+H2O=2Ce(OH)4+NaCl 2xCO+CeO2=CeO2(1-x)+2xCO2
【解析】考查化学工艺流程,(1)氧显-2价,C显+4价,F显-1价,整体化合价代数和为0,即Ce显+3价;(2)CeO2中Ce的化合价由+4价→+3价,CeO2作氧化剂,H2O2作还原剂,H2O2被氧化成O2,根据化合价升降法进行配平,其离子反应方程式为:2CeO2+H2O2+6H+=2Ce3++4H2O+O2↑;(3)该反应的离子方程式为Ce(BF4)3(s)+3K+(aq)=3KBF4(s)+Ce3+(aq),平衡常数K=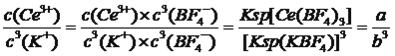 ;(4)随着c(SO42-)增大,水层中Ce4+被SO42-结合成[CeSO4]2+,c([CeSO4]2+)增大,同时导致Ce4++n(HA)2
;(4)随着c(SO42-)增大,水层中Ce4+被SO42-结合成[CeSO4]2+,c([CeSO4]2+)增大,同时导致Ce4++n(HA)2 ![]() Ce(H2n-4A2n)+4H+向左(逆向)移动,致使c[Ce(H2n-4A2n)]减小;(5)获得Ce(OH)3沉淀,c(OH-)=
Ce(H2n-4A2n)+4H+向左(逆向)移动,致使c[Ce(H2n-4A2n)]减小;(5)获得Ce(OH)3沉淀,c(OH-)=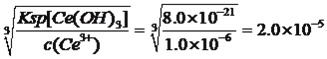 mol·L-1,pOH=-lgc(OH-)=4.7,即pH=9.3,pH应大于9.3;(6)NaClO作氧化剂,把Ce(OH)3氧化成Ce(OH)4,自身被还原成Cl-,根据化合价升降法进行配平,化学方程式为2Ce(OH)3+NaClO+H2O=2Ce(OH)4+NaCl;(7)根据信息,CO与氧气反应生成CO2,两式相加得到:2xCO+CeO2=CeO2(1-x)+2xCO2。
mol·L-1,pOH=-lgc(OH-)=4.7,即pH=9.3,pH应大于9.3;(6)NaClO作氧化剂,把Ce(OH)3氧化成Ce(OH)4,自身被还原成Cl-,根据化合价升降法进行配平,化学方程式为2Ce(OH)3+NaClO+H2O=2Ce(OH)4+NaCl;(7)根据信息,CO与氧气反应生成CO2,两式相加得到:2xCO+CeO2=CeO2(1-x)+2xCO2。

【题目】无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点231.9C)与Cl2 反应制备SnCl4装置如下图所示。
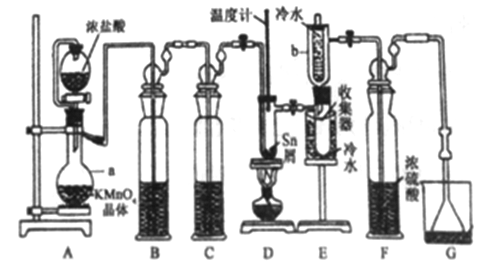
已知,① SnCl4在空气中极易水解生成SnO2xH2O;②SnCl2、SnCl4有关物理性质如下表。
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
回答下列问题:
(1)仪器a的名称是__________,其中发生反应的离子方程式为________。
(2)装置B、C 中盛装的试剂分别是_______、__________。
(3)当观察到装置F液面上方出现_____现象时才开始点燃酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的有:①加快氯气与锡反应,②__________。
(4)E装置中b的作用是___________。
(5)若制得产品中含有少量Cl2,则可采用下列_____(填字母)措施加以除去。
A.加入NaOH 萃取分液 B.加入足量锡再加热蒸馏
C.加入碘化钾冷凝过滤 D.加入饱和食盐水萃取
(6)可用滴定法测定最后产品的纯度。准确称取该样品mg加入到适量浓盐酸溶解,然后再加水稀释至250 mL,用移液管移取25.00 ml,稀释后的溶液于锥形瓶中,加入两滴淀粉溶液作指示制,用cmol/L 的KIO3 标准溶液进行滴定,平行滴定3 次,平均消耗V mL的标准溶液。已知滴定时发生的反应为:Sn2++IO3-+H+→Sn4++I2+H2O(未配平)。回答下列问题:
①判断达到滴定终点的现象为____________。
②产品中SnCl2(摩尔质量为M g/mol )的含量为____%(用含m、c、V、M 的代数式表示)。