题目内容
【题目】20℃时,在H2C2O4、NaOH混合溶液中,c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol/L。含碳元素微粒的分布分数δ随溶液pH变化的关系如图所示。下列说法正确的是
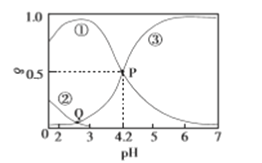
A. ①表示H2C2O4的分布曲线,③表示C2O42-的分布曲线
B. Q点对应的溶液中lgc(H+)<lgc(OH-)
C. 20℃时,H2C2O4的一级电离平衡常数Ka1=1×10-4.2
D. 0.100mol/L的NaHC2O4溶液中:c(OH-)=c(H+)- c(C2O42-)+c(H2C2O4)
【答案】D
【解析】A、随着溶液pH增大,溶液H2C2O4、HC2O4-先后被反应,越来越少,而C2O42-则越来越多,因此曲线①代表的是HC2O4-,②代表的是H2C2O4,③代表C2O42-,故A错误;B、Q点时溶液显酸性,因此c(H+)>c(OH-),即lgc(H+)>lgc(OH-),故B错误;C、电离平衡常数只受温度的影响,根据P点,Ka=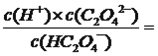 10-4.2,此平衡常数是草酸的二级电离,故C错误;D、根据质子守恒,因此有c(OH-)=c(H+)- c(C2O42-)+c(H2C2O4),故D正确。
10-4.2,此平衡常数是草酸的二级电离,故C错误;D、根据质子守恒,因此有c(OH-)=c(H+)- c(C2O42-)+c(H2C2O4),故D正确。

【题目】下列实验操作、实验现象和实验结论均正确的是
选项 | 实验操作 | 实验现象 | 实验结论 |
A | 将乙烯分别通入溴水和酸性高锰酸钾溶液 | 溶液均褪色 | 二者反应类型相同 |
B | 对于密闭烧瓶中的已达到平衡的可逆反应:2NO2 | 混合气体颜色变深 | 加热该化学平衡可向正向移动 |
C | 某溶液中加入新制氢氧化铜悬浊液,加热 | 有砖红色沉淀生成 | 该溶液一定是葡萄糖溶液 |
D | 甲烷和氯气混合气体充入大试管中,倒立在水槽里,置于光亮处,过一段时间后,将试管从水槽中取出,向其中滴入几滴石蕊溶液 | 溶液变红 | 甲烷和氯气反应产物中有氯化氢 |
A. AB. BC. CD. D