题目内容
【题目】A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图①所示:
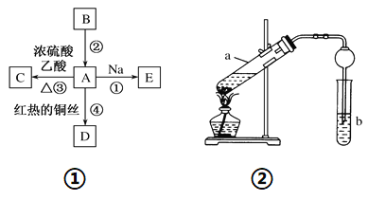
(1)写出B的结构简式________;A中能体现该物质性质的原子团的名称为______。
(2)写出下列反应的化学方程式:反应①________________;反应④________________。
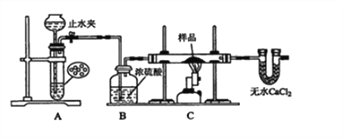
(3)实验室利用反应③制取C,常用图②装置:
①a试管中的主要化学反应的方程式为_________________,反应类型是______。
②在实验中球形干燥管除起冷凝作用外,另一个重要作用是________________。
③试管b中观察到的现象是______________________。
【答案】 CH2=CH2 羟基 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ 2CH3CH2OH+O2![]() 2CH3CHO+2H2O CH3COOH+CH3CH2OH
2CH3CHO+2H2O CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 酯化反应(或取代反应) 防倒吸 液体分层
CH3COOCH2CH3+H2O 酯化反应(或取代反应) 防倒吸 液体分层
【解析】B的产量可衡量一个国家石油化工发展的水平,则B是乙烯。A是化学实验室中常见的有机物,它易溶于水并有特殊香味,根据框图中信息,A能与Na、乙酸反应,在红热铜丝发生催化氧化,可推知A是乙醇。根据框图中的转化关系、反应条件和反应试剂可推得,C是乙酸乙酯,D是乙醛,E是乙醇钠,据此解答。
解析:(1)B是乙烯,结构简式为CH2=CH2,A是乙醇,能体现该物质性质的官能团是羟基。
(2)反应①是乙醇与钠反应生成乙醇钠与氢气,反应方程式为2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;反应④是乙醇的催化氧化,方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。
(3)①a试管中的主要化学反应是乙酸与乙醇发生酯化反应生成乙酸乙酯,化学方程式为CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O。
CH3COOCH2CH3+H2O。
②由于乙酸与乙醇均极易溶于水,则在实验中球形干燥管除起冷凝作用外,另一个重要作用是防止液体倒吸。
③由于乙酸乙酯不溶于水,则试管b中观察到的现象是液体分层。