题目内容
【题目】华为集团在通信网络、IT、智能终端和云服务等领域为客户提供有竞争力、安全可信赖的产品、解决方案与服务,与生态伙伴开放合作,持续为客户创造价值,释放个人潜能,丰富家庭生活,激发组织创新。华为坚持围绕客户需求持续创新,加大基础研究投入,厚积薄发,推动世界进步。其中MATE30手机采用锂离子电池,其正极材料为磷酸亚铁锂(LiFePO4),它具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。回答下列问题:
(1)在周期表中,与Li的化学性质最相似的邻族元素是________,该元素基态原子核外M层电子的自旋状态_______(填“相同”或“相反”)。
(2)FeCl3中的化学键具有明显的共价性(类似于氯化铝),蒸汽状态下以双聚分子存在的FeCl3的结构式为____,其中Fe的配位数为____。
(3)苯胺(![]() )的晶体类型是_____。苯胺与甲苯(
)的晶体类型是_____。苯胺与甲苯(![]() )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______。
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______。
(4)NH4H2PO4中,电负性最高的元素是______;其中PO43-采用_______杂化。
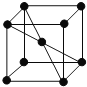
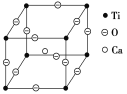
(5)如下图所示为高温超导领域里的一种化合物——钙钛矿的晶体结构,该结构是具有代表性的最小重复单位。该物质的化学式可表示为_____;若钙、钛、氧三元素的相对原子质量分别为a、b、c,晶体结构图中正方体边长(钛原子之间的距离)为d nm(1 nm=10-10Cm),则该晶体的密度为__g·cm-3。
【答案】Mg 相反 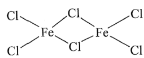 4 分子晶体 苯胺分子之间存在氢键 O SP3 CaTiO3
4 分子晶体 苯胺分子之间存在氢键 O SP3 CaTiO3 ![]() g/cm3
g/cm3
【解析】
该选修题涉及到了元素周期表和对角线原则、核外电子排布式的写法、配位物的形成,以及熔沸点的判断方式和分子晶体的判断方法。电负性的判断和杂化轨道的计算。
(1)根据元素周期表和对角线原则可知与Li化学性质相似的是Mg,Mg的最外层电子数是2,占据s轨道,s轨道最多容纳2个电子,所以自旋方向相反;
(2)氯化铁的双聚体,就是两个氯化铁相连接在一 起,已知氯化铁的化学键有明显的共价性所以仿照共价键的形式将两个氯化铁连接在一起, 即结构式为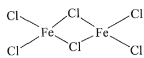 ,因此Fe的配位数为4;
,因此Fe的配位数为4;
(3)大多数有机物都是分子晶体,除了一部分有机酸盐和有机碱盐是离子晶体。苯胺比甲苯的熔沸点都高,同一种晶体类型熔沸点不同首先要考虑的就是是否有氢键,苯胺中存在电负性较强的N所以可以形成氢键,因此比甲苯的熔沸点高;
(4)电负性与非金属性的大小规律相似,从左到右依次增大,O就是最大的;
PO43-中价层电子对个数=4+![]() (5-5)=4,含孤电子对数为0,杂化轨道数4,所以原子杂化方式是sp3杂化;
(5-5)=4,含孤电子对数为0,杂化轨道数4,所以原子杂化方式是sp3杂化;
(5) )利用均摊法可以知道在每个晶胞中钛离子个数为8![]() =1,氧离子的个数为12
=1,氧离子的个数为12![]() ,钙离子个数为1,所以氧、钛、钙的离子个数比是3:1:1,化学式可表示为CaTiO3;
,钙离子个数为1,所以氧、钛、钙的离子个数比是3:1:1,化学式可表示为CaTiO3;
因为在每个晶胞中含有一个CaTiO3,根据![]() 可以知道密度为
可以知道密度为![]() =
= ![]() g/cm3。
g/cm3。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】已知![]() 时,
时,![]() 、HCN和
、HCN和![]() 的电离常数如表:
的电离常数如表:
| HCN |
|
|
|
|
下列有关叙述错误的是![]()
A.向NaCN溶液中通入少量![]() 的离子方程式:
的离子方程式:![]()
B.![]() 时,反应
时,反应![]() 的化学平衡常数为
的化学平衡常数为![]()
C.中和等体积、等物质的量浓度的![]() 和HCN溶液,消耗NaOH的量前者小于后者
和HCN溶液,消耗NaOH的量前者小于后者
D.等物质的量浓度的![]() 和NaCN混合溶液中:
和NaCN混合溶液中:![]()