题目内容
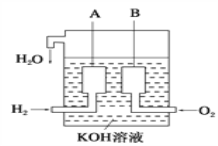
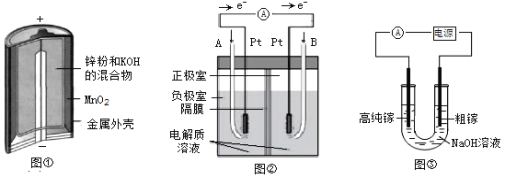
【题目】氮氧化物具有不同程度的毒性,利用构成电池方法既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,发生反应 6NO2+ 8NH3= 7N2+12H2O,装置如图所示。下列关于该电池的说法正确的是

A. 为使电池持续放电,离子交换膜需选用阴离子交换膜
B. 电子从右侧电极经过负载后流向左侧电极
C. 电极A极反应式为2NH3 - 6e-=N2 +6H+
D. 当有4.48LNO2被处理时,转移电子物质的量为 0.8mol
【答案】A
【解析】
由反应6NO2+8NH3=7N2+12H2O可知,反应中NO2为氧化剂,NH3为还原剂,则电极A为负极,电极B为正极。
A.A电极为负极,发生反应:2NH3-6e-+6OH-═N2+6H2O,由于OH-不断消耗,阴离子浓度降低,所以溶液中的OH-不断由正极区进入负极区,即离子交换膜为阴离子交换膜,A正确;
B.A电极为负极,电子从负极A电极经负载流向正极B电极,即从左侧电极经负载流向右侧电极,B错误;
C.A电极为负极,发生反应:2NH3-6e-+6OH-═N2+6H2O,在碱性溶液中不可能大量存在H+,C错误;
D.由于未指明气体所处的条件,所以不能根据气体体积确定气体的物质的量,也就不能确定电子转移数目,D错误;
故合理选项是A。

【题目】根据所学原理,完成下列各题
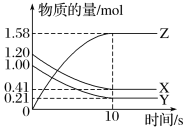
(1)从化学键的角度分析,化学反应的过程就是旧键断裂和新键的形成过程。已知反应:N2(g)+ 3H2(g)![]() 2NH3(g) △H=﹣93kJ/mol。试根据表中所列键能数据,计算a 的数值为____kJ/mol。
2NH3(g) △H=﹣93kJ/mol。试根据表中所列键能数据,计算a 的数值为____kJ/mol。
化学键 | H﹣H | N﹣H | N≡N |
键能/(kJ/mol) | 436 | a | 945 |
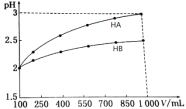
(2)25 ℃时,将a mol/L氨水与0.01 mol/L盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显________(填“酸”“碱”或“中”)性。用含a的代数式表示NH3·H2O的电离常数Kb=________。
(3)向含有BaSO4的饱和溶液中
①加入Na2SO4溶液,则c(Ba2+)__________(填“变大”、“变小”或“不变”,下同)。
②若改加更多的固体BaSO4,则c(Ba2+)将__________。
(4)目前已开发出用电解法制取ClO2的新工艺。

①图中用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为___________。
②电解一段时间,当阴极产生的气体体积为112 mL (标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为________mol。