��Ŀ����
����Ŀ���绯ѧԭ��������ת��������ұ���ȷ���Ӧ�ù㷺��
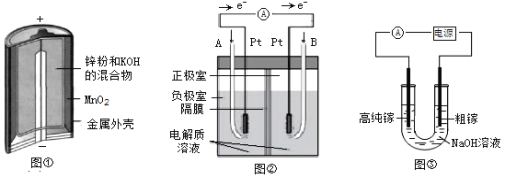
��1��ͼ���Ǽ���п�̵�أ��ڸ���������Ӧ��������__________������Zn������MnO2��������������_________��Ӧ������������������ԭ������
��2��ͼ���Ǽ��Ե���ʵ�����ȼ�ϵ�أ�B��ͨ�������Ϊ________��A�������ĵ缫��Ӧʽ____________________________________________��
��3����ⷨ�����ᴿ���أ�����ԭ����ͼ����ʾ��
�ٴ������Դ___________����������������������������
�����������ܽ����ɵ�Ga3+��NaOH��Һ��Ӧ����GaO2����GaO2���������ŵ�ĵ缫��Ӧʽ______________________________________________________��
��4������������ұ����Ӧ����������õ�ⷨ����________(ѡ����ĸ���)��
a��NaCl b��Fe2O3���� c��Cu2S���� d��Al2O3
���𰸡�Zn ��ԭ O2 H2-2e-+2OH-=2H2O �� GaO2-+3e-+2H2O=Ga+4OH- ad
��������
����ԭ��ء����صĹ���ԭ���Լ��缫��Ӧ����ʽ����д���������𣻸��ݳ���������ұ�������������
(1) ͼ���Ǽ���п�̵�أ����ý���п������������������Ӧ��MnO2��������������ԭ��Ӧ��
�ʴ�Ϊ��Zn����ԭ��
(2)ȼ�ϵ���е��ӴӸ���������������A�缫�����Ǹ�����B�缫������������ȼ������������A�缫ͨ��H2��B�缫ͨ��O2��A�������ĵ缫��ӦΪ��H2-2e-+ 2OH-=2H2O��B�缫�����ĵ缫��ӦΪ��O2+4H2O+4e-=4OH-��
�ʴ�Ϊ��O2��H2-2e-+ 2OH-=2H2O��
(3) �ٵ�ⷨ�ᴿ����ʱ��������������ʧȥ���ӣ���������Դ����������
�ʴ�Ϊ��������
�����������ܽ����ɵ�Ga3+��NaOH��Һ��Ӧ����GaO2�����÷�Ӧ�����ӷ���ʽΪ��Ga3+��4OH-��GaO2-+2H2O��GaO2���������ŵ�ʱ�õ���������Ga�ĵ缫��Ӧ��
�ʴ�Ϊ��GaO2-+3e-+2H2O=Ga+4OH-��
(4)��ⷨһ��Ӧ���ڻ��ý����ĵ�ұ�������磺�����ء��ơ�þ������ұ����
�ʴ�Ϊ��ad��