题目内容
19.下列各组物质相互反应时,改变反应的条件或者反应物的物质的量之比,生成的产物不变的是( )| A. | Na与氧气 | B. | 澄清石灰水与二氧化碳 | ||
| C. | 碳与氧气 | D. | 过氧化钠和水 |
分析 钠与氧气反应产物与反应条件有关,澄清石灰水与二氧化碳、碳与氧气二者反应产物与反应物用量有关,过氧化钠和水反应生成氢氧化钠和氧气,据此解答.
解答 解:A.Na与氧气在常温下生成氧化钠,在加热或者点燃条件下生成过氧化钠,产物与反应条件有关,故A不选;
B.澄清石灰水与二氧化碳,二氧化碳少量生成碳酸钙,二氧化碳过量生成碳酸氢钙,产物与反应物用量有关,故B不选;
C.碳与氧气,氧气足量生成二氧化碳,氧气不足生成一氧化碳,产物与反应物用量有关,故C不选;
D.过氧化钠和水生成氢氧化钠和氧气,改变反应的条件或者反应物的物质的量之比,生成的产物不变,故D选;
故选:D.
点评 本题考查了反应物间反应条件或反应物用量与反应产物的联系,题目难度不大,注意把握常见元素化合物的性质.

练习册系列答案
相关题目
20.实验中的下列操作正确的是( )
| A. | 取用试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | 把NaOH固体放在托盘天平左盘的滤纸上称量 | |
| C. | 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| D. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
7. 如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:X(g)+3Y(g)?2Z(g)△H=-192kJ•mol-1.向M、N中都通入a mol X和b mol Y的混合气体,初始时M、N两容器的容积相同,保持两容器的温度相同且恒定不变.下列说法一定正确的是( )
如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:X(g)+3Y(g)?2Z(g)△H=-192kJ•mol-1.向M、N中都通入a mol X和b mol Y的混合气体,初始时M、N两容器的容积相同,保持两容器的温度相同且恒定不变.下列说法一定正确的是( )
 如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:X(g)+3Y(g)?2Z(g)△H=-192kJ•mol-1.向M、N中都通入a mol X和b mol Y的混合气体,初始时M、N两容器的容积相同,保持两容器的温度相同且恒定不变.下列说法一定正确的是( )
如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:X(g)+3Y(g)?2Z(g)△H=-192kJ•mol-1.向M、N中都通入a mol X和b mol Y的混合气体,初始时M、N两容器的容积相同,保持两容器的温度相同且恒定不变.下列说法一定正确的是( )| A. | 平衡时,X的体积分数:M<N | |
| B. | 若向N中再充入a mol X和b mol Y,则平衡时,X的转化率:M<N | |
| C. | 若a:b=1:3,当M中放出172.8 kJ热量时,X的转化率为90% | |
| D. | 若a=1.2,b=1,并且N中达到平衡时体积为2 L,此时含有0.4 mol Z,则再通入0.36 mol X时,v(正)<v(逆) |
4.在水溶液中,下列电离方程式正确的是( )
| A. | CH3COOH═CH3COO-+H+ | B. | NaHSO4═Na++HSO4- | ||
| C. | HCO3-═H++CO32- | D. | HPO4-?H++PO43- |
11.下列仪器有“0”刻度且“0”刻度位置正确的是( )
| A. | 在量筒的下端 | B. | 在温度计的中部 | ||
| C. | 在托盘天平刻度尺的中间 | D. | 在容量瓶的上端 |
8.下列实验操作正确的是( )
| A. | 蒸馏操作时,温度计水银球应插入到液体中 | |
| B. | 萃取操作时,应选择溶质在其中更易溶的溶剂作萃取剂,且萃取剂与原溶剂互不相溶,其密度比原溶剂要大 | |
| C. | 用固体NaOH配制一定物质的量浓度的NaOH溶液,将NaOH固体溶于水后,立即将溶液转移到容量瓶中 | |
| D. | 称取28.6gNa2CO3•10H2O溶于水配制成100 mL1mol•L-1的Na2CO3溶液 |
9.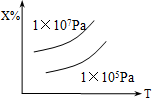 已知X(g)+2Y(g)?nZ的反应达到平衡状态时,体系中X的质量分数与温度(T),压强的关系如下图所示,下列说法中正确的是( )
已知X(g)+2Y(g)?nZ的反应达到平衡状态时,体系中X的质量分数与温度(T),压强的关系如下图所示,下列说法中正确的是( )
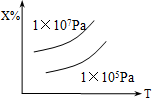 已知X(g)+2Y(g)?nZ的反应达到平衡状态时,体系中X的质量分数与温度(T),压强的关系如下图所示,下列说法中正确的是( )
已知X(g)+2Y(g)?nZ的反应达到平衡状态时,体系中X的质量分数与温度(T),压强的关系如下图所示,下列说法中正确的是( )| A. | Z是气态,n=3,正反应△H<0 | B. | Z是气态,n>3,正反应△H<0 | ||
| C. | Z是气态,n=3,正反应△H>0 | D. | Z不是气态,n<3,正反应△H>0 |
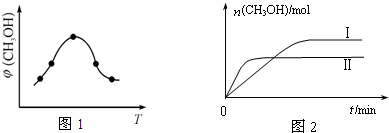
 CO(NH2)2+H2O.开始以氨碳比$\frac{n(N{H}_{3})}{n(C{O}_{2})}$=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为40%.
CO(NH2)2+H2O.开始以氨碳比$\frac{n(N{H}_{3})}{n(C{O}_{2})}$=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为40%.