��Ŀ����
14��������ԭ��Ӧ�ġ�������Ԫ�صĻ��ϼ��б仯���������е��ӵ�ת�ƣ����������3�⣮��1�����������ð�ˮ����ܵ��Ƿ�©�������䷴ӦʽΪ3Cl2+8NH3�T6NH4Cl+N2������160.5gNH4Cl����ʱ���������İ�����17g��
��2������Ȼ�磬��Ȼˮ�еġ�����������˾��������ÿ����е��������ر��Ļ�������Ҫ�ɷ�ΪFeS2������Ϊ����������ʹˮ��������ǿ���÷�Ӧ���̵Ļ�ѧ����ʽΪ4FeS2+15O2+2H2O$\frac{\underline{\;ϸ��\;}}{\;}$2Fe2��S04��3+2H2S04����������������ˮ����ͭ��ʯ����ʱ����ʹCu2S�ܽ⣬ˮ�����Խ�һ����ǿ����Ӧ�����ӷ���ʽ���£�����ƽ֮��10Fe3++1Cu2S+4H2O�T10Fe2++2Cu2++8H++1SO42-
��3����ɲ���ƽ���·�Ӧ�Ļ�ѧ����ʽ��
��ʵ������������MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2����
��ʵ���Ҽ��ȸ��������������2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$ K2MnO4+MnO2+O2����
�۰ѹ�������Ͷ��ˮ�������繩����2CaO2+2H2O�T2Ca��OH��2+O2����
���� ��1��3Cl2+8NH3�T6NH4Cl+N2�У�ClԪ�صĻ��ϼ۽��ͣ�NԪ�صĻ��ϼ����ߣ����Ԫ�ػ��ϼ۵ı仯�Լ���Ӧ�ķ���ʽ���
��2����Ӧ��ΪFeS2��������ˮ��������ΪFe2��S04��3�����ᣬ���ݷ�Ӧ�����������д��ѧ��Ӧ����ʽ��
Cu2S��CuԪ�صĻ��ϼ���+1����Ϊ+2��SԪ�صĻ��ϼ���-2����Ϊ+6��FeԪ�صĻ��ϼ���+3�۽���Ϊ+2������ת�Ƶ����غ㡢ԭ���غ���ƽ����ʽ��
��3����ʵ�����������ö���������Ũ������������Ȼ��̡�������ˮ��
��ʵ���Ҽ��ȸ��������������ء��������̺�������
�۰ѹ�������Ͷ��ˮ�з�����Ӧ�����������ƺ�������
��� �⣺��1��n��NH4Cl��=$\frac{160.5g}{53.5g/mol}$=3mol��
3Cl2+8NH3=6NH4Cl+N2��������NH3
3 8 6 2
3 x
x=1mol��
�������İ���������Ϊ1mol��17g/mol=17g��
�ʴ�Ϊ��17��
��2����Ӧ��ΪFeS��������ˮ��������ΪFe2��S04��3�����ᣬ������Ӧ�Ļ�ѧ����ʽΪ4FeS2+15O2+2H2O$\frac{\underline{\;ϸ��\;}}{\;}$2Fe2��S04��3+2H2S04��Cu2S��CuԪ�صĻ��ϼ���+1����Ϊ+2��SԪ�صĻ��ϼ���-2����Ϊ+6��FeԪ�صĻ��ϼ���+3�۽���Ϊ+2���پݵ���غ�ȷ������ΪH+��������ӷ�ӦΪCu2S+10Fe3++4H2O$\frac{\underline{\;ϸ��\;}}{\;}$2Cu2++10Fe2++8H++S042-��
�ʴ�Ϊ��4FeS2+15O2+2H2O$\frac{\underline{\;ϸ��\;}}{\;}$2Fe2��S04��3+2H2S04�� 10��1��4H2O��10��2��8��1��
��3����ʵ�����������ö���������Ũ����������ɣ�����ʽΪ��MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2�����ʴ�Ϊ��MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2����
��ʵ���Ҽ��ȸ��������������ء��������̺�����������ʽΪ��2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$ K2MnO4+MnO2+O2�����ʴ�Ϊ��2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$ K2MnO4+MnO2+O2����
�۰ѹ�������Ͷ��ˮ�з�����Ӧ�����������ƺ�����������ʽΪ��2CaO2+2H2O�T2Ca��OH��2+O2�����ʴ�Ϊ��2CaO2+2H2O�T2Ca��OH��2+O2����
���� ���⿼��������ԭ��Ӧ��Ϊ��Ƶ���㣬��ȷ�����ķ�Ӧ����Ӧ��Ԫ�صĻ��ϼ۱仯���ɽ�𣬲��ط�����Ӧ�������Ŀ��飬��Ŀ�ѶȲ���

| A�� | ���ó���ʯ��ˮ�����ֶ�����̼�Ͷ������� | |
| B�� | ������ˮ����ͭ����ƾ����Ƿ�����ˮ | |
| C�� | ��ʹ���ȵ�CuO�ɺڱ�������һ����H2 | |
| D�� | ����ʯ����Һ����������ʹ��� |
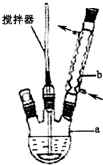 ����ȩ��Ũ����������ܷ����绯��Ӧ���ɱ��״��ͱ������Σ�ijʵ��С�����ø�ԭ���Ʊ������ı����ᣮ
����ȩ��Ũ����������ܷ����绯��Ӧ���ɱ��״��ͱ������Σ�ijʵ��С�����ø�ԭ���Ʊ������ı����ᣮ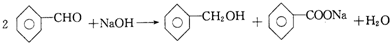
����������ף������õ����й��������£�
��1���й����ʵ��ܶȡ��е㡢�ܽ���
| ���� | ����Է��� ���� | �ܶ�/ �������ˮ�� | �����е�/�� | ���������ܽ��� |
| ����ȩ | 106 | 1.046 | 178.8 | ����ˮ���ɻ������Ҵ������ѡ������ȷ� |
| ���״� | 108 | 1.042 | 205.7 | ����ˮ���������Ҵ����ѡ����� |
| ������ | 122 | 1.271 | 249.2 | ����ˮ���������Ҵ������ѡ��ȷ¡���������̼�����Ȼ�̼ |
| ���������� | 144 | 1.442 | 249.3 | ����ˮ���Ҵ������͡������״����������� |
| �¶�/�� | 25 | 50 | 95 |
| �ܽ��/g | 0.17 | 0.95 | 6.8 |
��1��д��װ��ͼ�в������������ƣ�a������ƿ��b�����Σ������ܣ�
��2��Ϊ�˽�һ���ᴿ�����ᣬͨ�������ؽᾧ�����У��ڽ��и�ʵ���������Ҫ���ȹ��ˣ����ֱ�����ȫ�ܺ�������Ҫ�ټ�����������ˮ��Ŀ����Ϊ�˼��ٳ��ȹ��˹�������ʧ�����ᣮ
��3����������IJ�Ʒ����ϴ�ӡ�������龭����������õ����Ƿ��Ǵ����ı�����ij��÷����Dzⶨ��ò�Ʒ���۵��Ƿ���122.4�森
��4�������������У�������ȩ��ȡ������Ϊ2.120g�����ջ�ȡ�Ĵ��������������Ϊ1.098g������IJ���Ϊ90.0%��
��5��ijͬѧ��Ϊ�ɴ���ȥ����ȡ�л����л�ȡ���״���Ϊ��ɸ�ʵ����Ҫ�IJ����������¶ȼơ�β�ӹܼ�������ƿ��ֱ�������ܡ���ƿ��
| A�� | Na������ | B�� | ����ʯ��ˮ�������̼ | ||
| C�� | ̼������ | D�� | �������ƺ�ˮ |
| ѡ�� | ���� | ���� | ���� |
| A | ��Ũ����ε����DZ��� | ���������� | Ũ��������ˮ�Ժ�ǿ������ |
| B | ��һ��Al���ھƾ��ƻ��������� | Al�����ڶ������� | Al����������Ӧ |
| C | ��һС��Na��������ͭ��Һ�� | ��ͭ�������� | Na���û�������ͭ�е�ͭ |
| D | ��ˮ����ͨ�����ȵ����� | ��ĩ��� | ����ˮ�ڸ����·�����Ӧ |
| A�� | A | B�� | B | C�� | C | D�� | D |
 ij��ѧ��ȤС����ݷ�Ӧ��Mg+H2SO4�TMgSO4+H2����Ʋⶨþԭ��Ħ��������ʵ�飬ʵ��ļ���װ����ͼ����ȥ��������Ĥ��þ��������Ϊ0.24g��þ����ȫ��Ӧ������Ͳ�ռ�ˮ�����Ϊ0.224L�������ۻ��ɱ�״���µĶ�Ӧ����������������й��ڸ�ʵ������������ȷ���ǣ�������
ij��ѧ��ȤС����ݷ�Ӧ��Mg+H2SO4�TMgSO4+H2����Ʋⶨþԭ��Ħ��������ʵ�飬ʵ��ļ���װ����ͼ����ȥ��������Ĥ��þ��������Ϊ0.24g��þ����ȫ��Ӧ������Ͳ�ռ�ˮ�����Ϊ0.224L�������ۻ��ɱ�״���µĶ�Ӧ����������������й��ڸ�ʵ������������ȷ���ǣ�������| A�� | ʵ��ǰӦ����װ�õ������� | |
| B�� | װ�����е�ˮ��������NaCl��Һ���� | |
| C�� | ����ʱ��Ӧʹװ���Һ�װ�ñ��е�Һ�洦��ͬһˮƽ���� | |
| D�� | þԭ�ӵ�Ħ������Ϊ24.0 g��mol-1 |
 A��B��C�����ձ��зֱ�ʢ����ͬ���ʵ���Ũ�ȵ�ϡ���ᣬ��ͼ��ʾ��
A��B��C�����ձ��зֱ�ʢ����ͬ���ʵ���Ũ�ȵ�ϡ���ᣬ��ͼ��ʾ��
 �����ճ���������;��㡢�������Ľ������ϣ�
�����ճ���������;��㡢�������Ľ������ϣ�