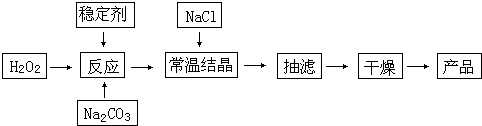
��Ŀ����
12����������ƣ�Na2S2O3����������ͳ����ҵ�Ķ�Ӱ��������ʱ�ظ����εĻ�ԭ����ֽ��Ư��ʱ�����ȼ��ȣ�ij��ѧ̽��С��ͨ���������ϣ�����ͼ1��ʾװ�ü��Լ����Ʊ���������ƣ�
��1��װ��A�еġ����ᡱ���ѡ��C������ĸ��ţ���
A���������� B��Ũ���� C��80%������ D��10%������
��2��װ��C�г�����Ŀ���������������⣬������һ���������壮��װ��C�з�����Ӧ�����ӷ���ʽΪ4SO2+2S2-+CO32-�T3S2O32-+CO2��
��3��װ��B�������Ƿ�ֹװ��C�е�Һ�嵹����װ��A�У�������ȫƿ����װ��D������������β���е�SO2��
��4��������Һ©���е����ỻΪŨ���ᣬװ��C�г���������������⣬������һ�����Σ������εĻ�ѧʽΪNaCl��Ϊ��ֹ�����ε����ɣ���ͬѧ������װ������������ͼ2װ��E����װ��EӦ�����ӵ�λ��ΪA������ĸ��ţ���
A��ֻ����װ��A��װ��B֮��
B��ֻ����װ��B��װ��C֮��
C����װ��A��װ��B��װ��B��װ��C֮�䶼����
D��ֻ����װ��C��װ��D֮��
��װ����ʢ�ŵ��Լ�ΪD������ĸ��ţ���
A��NaOH��Һ B��Na2SO3��Һ C��NaHCO3��Һ D��NaHSO3��Һ��
���� �������������Ʒ�Ӧ����SO2��װ��B�е��������ܾ�Ϊ�̹ܣ�����ȫƿ��װ��C�ж����������ƺ�̼���Ʒ�Ӧ������������ƺͶ�����̼��װ��D�е�����������Һ�������������Ӧ����ֹ��Ⱦ������
��1��SO32-��H+��Ӧ������SO2��������������Ƿ���״̬�����ᣬ�����ܵ����H+��
��2����Ϸ�Ӧ��̼���ƿ�֪���ɵ���������Ϊ������̼����˸÷�Ӧ�ķ�Ӧ��Ϊ�����������ƺ�̼���ƣ�������Ϊ��������ƺͶ�����̼��
��3��װ��B�е��������ܾ�Ϊ�̹ܣ�����ȫƿ��װ��D�е�����������Һ�������������Ӧ��
��4���������ỻΪŨ���ᣬ�����ɵĶ��������л��� HCl��װ�� E �������dz�ȥ HCl������Ӧ�����ڰ�ȫƿǰ�� �����������������ơ��������ơ�̼��������Һ���ܷ�����Ӧ��
��� �⣺�������������Ʒ�Ӧ����SO2��װ��B�е��������ܾ�Ϊ�̹ܣ�����ȫƿ��װ��C�ж����������ƺ�̼���Ʒ�Ӧ������������ƺͶ�����̼��װ��D�е�����������Һ�������������Ӧ����ֹ��Ⱦ������
��1��SO32-��H+��Ӧ������SO2��������������Ƿ���״̬�����ᣬ�����ܵ����H+�������Ũ�ȴ���Ӧ���ʿ죬��ѡȡ80%�����ᣬ�ʴ�Ϊ��C��
��2����Ϸ�Ӧ��̼���ƿ�֪���ɵ���������Ϊ������̼����˸÷�Ӧ�ķ�Ӧ��Ϊ�����������ƺ�̼���ƣ�������Ϊ��������ƺͶ�����̼�����ӷ���ʽΪ��4SO2+2S2-+CO32-�T3S2O32-+CO2���ʴ�Ϊ��4SO2+2S2-+CO32-�T3S2O32-+CO2��
��3��װ��B�е��������ܾ�Ϊ�̹ܣ�����ȫƿ��װ��D�е�����������Һ�������������Ӧ����ֹ��Ⱦ�������ʴ�Ϊ����ֹװ��C�е�Һ�嵹����װ��A�У�������ȫƿ��������β���е�SO2��
��4���������ỻΪŨ���ᣬ�����ɵĶ��������л��� HCl��HCl ����̼���ơ����Ʒ�Ӧ�����Ȼ��ƣ�װ�� E �������dz�ȥ HCl������Ӧ�����ڰ�ȫƿǰ�� �����������������ơ��������ơ�̼��������Һ���ܷ�����Ӧ�����ֻ��ѡȡ NaHSO3��Һ���ʴ�Ϊ��NaCl��A��D��
���� ���⿼���������Ʊ�ʵ�鷽������ƺ��Ʊ����̷���Ӧ�ã���Ҫ��ʵ�����������Ӧ�ã����ջ�����ע������ǽ���ؼ�����Ŀ�Ѷ��еȣ�

| A�� | ̼������Һ�м������������CO32-+2CH3COOH�TCO2��+H2O+2CH3COO- | |
| B�� | ��������Һ��ͨ��������CO2��2C6H5O-+CO2+H2O��2C6H5OH+CO32- | |
| C�� | ��������Һ�е���NaOH��Һ��H2NCH2COOH+OH-��H2NCH2COO-+H2O | |
| D�� | ���Ȼ�����Һ�м�������������2Fe3++Fe=3Fe2+ |
| A�� | 35% | B�� | 70% | C�� | 17.5% | D�� | 0.035% |
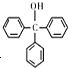 ����һ����Ҫ�Ļ���ԭ�Ϻ�ҽҩ�м��壬ʵ���Һϳ������״��ĺϳ�������ͼ1��ʾ��װ����ͼ2��ʾ
����һ����Ҫ�Ļ���ԭ�Ϻ�ҽҩ�м��壬ʵ���Һϳ������״��ĺϳ�������ͼ1��ʾ��װ����ͼ2��ʾ��֪����i�������Լ�����ˮ�⣬
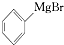 +H2O��
+H2O�� +M��OH��Br����ʽ�廯þ��
+M��OH��Br����ʽ�廯þ������������ʵ������������£�
| ���� | �۵� | �е� | �ܽ��� |
| �����״� | 164.2�� | 380�� | ������ˮ�������Ҵ������ѵ��л��ܼ� |
| ���� | -116.3�� | 34.6�� | ����ˮ�������Ҵ��������л��ܼ� |
| �屽 | -30.7�� | 156.2�� | ������ˮ�������Ҵ������ѵȶ����л��ܼ� |
| ���������� | -34.6�� | 212.6�� | ������ˮ |
| Mg��OH��Br | ������Ϊ���� | ������ˮ�������Ҵ����ѵȶ����л��ܼ� | |
�й̶��۵㣮
��ش��������⣺
��1��ͼ2�в�������B�����ƣ������ܣ�װ����ˮCaCl2������A�������Ƿ�ֹ�����е�ˮ��������װ�ã���������Լ�ˮ�⣮
��2��ͼ2�еμ�Һ��δ����ͨ��Һ©�����ú�ѹ��Һ©����������ƽ��ѹǿ��ʹ©����Һ��˳�����£���ȡ�����Լ�ʱҪ�����У����Բ���ˮԡ���ȷ�ʽ��
��3���Ƶõ������״��ֲ�Ʒ�У��������ѡ��屽���������������л���ͼ�ʽ�廯þ�����ʣ�������������ᴿ����������д���¿հף�
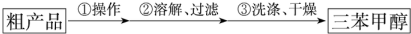
���У��ٲ���Ϊ����������ϴ��Һ���ѡ��a��������ѡ����ѡ��
A��ˮ B������ C���Ҵ� D����
�����Ʒ�Ѿ�ϴ�Ӹɾ��IJ���Ϊ��ȡ�������һ��ϴ��Һ���Թ��У��μ���������Һ�����������ɣ����Ѿ�ϴ�Ӹɾ�����֮��δϴ�Ӹɾ���
��4�����Ȳⶨ����ȡ2.60g��Ʒ�����������Һ���������������ƣ��������Ʋ���Ӧ������ַ�Ӧ������ɵ������ڱ�״���µ����Ϊ100�� 80mL�����Ʒ�������״�����������Ϊ90%��
�ٷ��ȷ�Ӧ�ڳ����¾����Է����У� �ڵ������У���ѧ��ת��Ϊ���ܶ������桱������
��ԭ��ع���ʱ�������ķ�Ӧһ����������ԭ��Ӧ�� �ܼ���ʱ�����ȷ�Ӧ��v���������С��
��������ܷ���ˮ�ⷴӦ�� ��ѧƽ�ⳣ���ı���ʽ�뻯ѧ��Ӧ����ʽ����д�أ�
| A�� | �٢ڢܢݢ� | B�� | �٢ܢݢ� | C�� | �ڢۢݢ� | D�� | �٢ڢܢ� |
| A�� | IA����VIIA��Ԫ�ؼ���γɹ��ۻ���������ӻ����� | |
| B�� | ��������Ԫ�ش����ң�������۴�+1 ������+7 | |
| C�� | ͬ����Ԫ�صļ������ӻ�ԭ��Խǿ������ˮ��Խ����ˮ�� | |
| D�� | ͬ���ڵ��������Ԫ�صĻ��ϼ�Խ�ߣ���ԭ��ʧ��������Խ�� |
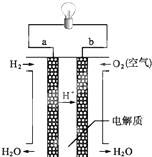 ����Ӧ��ԭ���ԭ�������˶��ֵ�أ������㲻ͬ����Ҫ������ÿС���еĵ�ع㷺ʹ�����ճ���������Ϳ�ѧ�����ȷ��棬����������ṩ����Ϣ����д�ո�
����Ӧ��ԭ���ԭ�������˶��ֵ�أ������㲻ͬ����Ҫ������ÿС���еĵ�ع㷺ʹ�����ճ���������Ϳ�ѧ�����ȷ��棬����������ṩ����Ϣ����д�ո�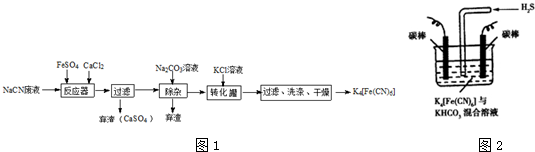
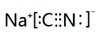 ��
��