题目内容
能正确表示下列反应的离子方程式是( )
| A、Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
| B、用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+═Cu2++2H2O |
| C、硫酸亚铁溶液中加入酸化的双氧水:Fe2++2H++H2O2═Fe3++2H2O |
| D、用惰性电极电解熔融氯化钠:2Cl-+2H2O═Cl2↑+H2↑+2OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.三价铁离子能够氧化碘离子;
B.双氧水具有强的氧化性,在酸性条件下能够氧化铜;
C.电荷不守恒;
D.不符合反应的客观事实,用惰性电极电解熔融氯化钠,得到氯气和钠.
B.双氧水具有强的氧化性,在酸性条件下能够氧化铜;
C.电荷不守恒;
D.不符合反应的客观事实,用惰性电极电解熔融氯化钠,得到氯气和钠.
解答:
解:A.Fe(OH)3溶于氢碘酸中,离子方程式为:2Fe(OH)3+6H++2I-=2Fe2++6H2O+I2,故A错误;
B.用双氧水和稀硫酸处理印刷电路板,离子方程式:Cu+H2O2+2H+═Cu2++2H2O,故B正确;
C.硫酸亚铁溶液中加入酸化的双氧水,离子方程式为:2Fe2++2H++H2O2═2Fe3++2H2O,故C错误;
D.用惰性电极电解熔融氯化钠,离子方程式为:2Na++2Cl-
2Na+Cl2↑,故D错误;
故选:B.
B.用双氧水和稀硫酸处理印刷电路板,离子方程式:Cu+H2O2+2H+═Cu2++2H2O,故B正确;
C.硫酸亚铁溶液中加入酸化的双氧水,离子方程式为:2Fe2++2H++H2O2═2Fe3++2H2O,故C错误;
D.用惰性电极电解熔融氯化钠,离子方程式为:2Na++2Cl-
| ||
故选:B.
点评:本题考查了离子方程式的书写,明确反应的实质是解题关键,注意D为易错选项,电解熔融的氯化钠得到钠和氯气.

练习册系列答案
相关题目
已知pH=2的高碘酸(H5IO6)溶液与pH=12的NaOH溶液等体积混合,所得混合液显酸性;0.01mol?L-1的碘酸(HIO3)溶液与pH=12的NaOH溶液等体积混合,所得混合液显中性.下列对高碘酸和碘酸的酸性强弱判断正确的是( )
| A、高碘酸和碘酸都是强酸 |
| B、高碘酸和碘酸都是弱酸 |
| C、高碘酸是弱酸,碘酸是强酸 |
| D、高碘酸是强酸,碘酸是弱酸 |
设NA代表阿伏加德罗常数,以下说法不正确的是( )
| A、18g水中含有电子数为10NA |
| B、16g氧气所含原子数为NA |
| C、4.8g金属镁变成镁离子时失去电子数为0.2NA |
| D、46g二氧化氮和46g四氧化二氮含有的原子数均是3NA |
对于反应14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4来说,下列结论正确的是( )
| A、FeS2既是氧化剂,又是还原剂 |
| B、只有CuSO4作氧化剂 |
| C、被氧化的硫和被还原的硫质量比是3:7 |
| D、被氧化的硫和被还原的硫质量比是1:1 |
正确的实验设计和操作是实验成功的重要因素,下列实验设计或操作正确的是( )
A、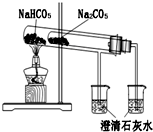 证明热稳定性Na2CO3>NaHCO3 |
B、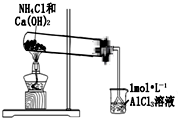 证明氢氧化铝的两性 |
C、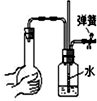 检查装置气密性 |
D、 测定KClO3元素的质量 |
设NA为阿伏加德罗常数的值,下列说法正确的组合是( )
| A、常温下,1mol/L的NH4NO3溶液中含有氮原子的数目为2NA |
| B、17g H2O2中含有的电子数为9NA |
| C、将2mol SO2与1mol O2混合,发生反应转移的电子总数一定是4NA |
| D、常温下,100mL 1mol?L-1 AlCl3溶液中铝离子数为0.1NA |
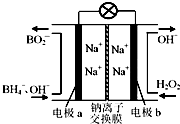 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )| A、电池放电时Na+从a极区移向b极区 |
| B、每消耗3mol H2O2,转移的电子为3mol |
| C、电极a采用MnO2,MnO2既作电极材料又有催化作用 |
| D、该电池的负极反应为:BH4-+8OH--8e-═BO2-+6H2O |
下列各装置中,烧杯中盛有海水,能够形成原电池并且铁为正极的是( )
A、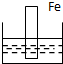 |
B、 |
C、 |
D、 |