题目内容
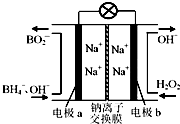 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )| A、电池放电时Na+从a极区移向b极区 |
| B、每消耗3mol H2O2,转移的电子为3mol |
| C、电极a采用MnO2,MnO2既作电极材料又有催化作用 |
| D、该电池的负极反应为:BH4-+8OH--8e-═BO2-+6H2O |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:由原电池工作原理示意图可知反应中BH4-被氧化为BO2-,应为原电池的负极反应,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,正极H2O2得电子被还原生成OH-,电极反应式为H2O2+2e-=2OH-,原电池工作时,阳离子向正极移动,阴离子向负极移动,以此解答该题.
解答:
解:A.BH4-被氧化为BO2-,应为原电池的负极反应,正极H2O2得电子被还原生成OH-,原电池工作时,阳离子向正极移动,则电池放电时Na+从a极区移向b极区,故A正确;
B.每消耗3molH2O2,转移的电子为6mol,故B错误;
C.电极a采用Pt/C,为原电池的负极,故C错误;
D.BH4-被氧化为BO2-,应为原电池的负极反应,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,故D正确.
故选AD.
B.每消耗3molH2O2,转移的电子为6mol,故B错误;
C.电极a采用Pt/C,为原电池的负极,故C错误;
D.BH4-被氧化为BO2-,应为原电池的负极反应,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,故D正确.
故选AD.
点评:本题考查原电池的工作原理,为高频考点,侧重于学生的分析能力的考查,题目难度中等,本题注意根据物质化合价的变化判断两极反应为解答该题的关键,注意电极反应式的书写.

练习册系列答案
相关题目
某高分子化合物是制造彩电荧光屏的原料之一,其结构简式为: ,下列有关该高分子化合物的说法不正确的是( )
,下列有关该高分子化合物的说法不正确的是( )
 ,下列有关该高分子化合物的说法不正确的是( )
,下列有关该高分子化合物的说法不正确的是( )| A、不易溶于水 |
| B、可以发生酯化反应 |
| C、可以发生加成反应 |
| D、水解后能得到分子式为C9H8O2的产物 |
能正确表示下列反应的离子方程式是( )
| A、Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
| B、用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+═Cu2++2H2O |
| C、硫酸亚铁溶液中加入酸化的双氧水:Fe2++2H++H2O2═Fe3++2H2O |
| D、用惰性电极电解熔融氯化钠:2Cl-+2H2O═Cl2↑+H2↑+2OH- |
下列有关说法正确的是( )
| A、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H>0 | ||
| B、电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | ||
C、CH3COOH溶液加水稀释后,溶液中
| ||
| D、Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
下列说法正确的是( )
| A、液氯比氯水有更强的漂白性 |
| B、实验室Cl2时,可用饱和Na2CO3溶液除去其中的HCl |
| C、新制氯水应保存在棕色试剂瓶中 |
| D、漂白粉的有效成分是CaCl2和Ca(ClO)2 |
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30).A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个未成对电子;E的原子序数为28;D与E同周期,价电子数为2.则下列说法正确的是( )
| A、元素A、B、C的氢化物的稳定性顺序:A>B>C |
| B、元素A、B、C、D的原子半径大小顺序:D>A>B>C |
| C、元素E的基态原子的外围电子排布式:3d10 |
| D、元素B、C、D形成的化合物DB2和DC2都是离子化合物,且阴阳离子数之比都为2:1 |
下列物质按照混合物、非电解质、碱、酸式盐的顺序排列正确的是( )
| A、漂白粉、Cl2、氨水、NaHCO3 |
| B、福尔马林、苯、Cu2(OH)2CO3、明矾 |
| C、食醋、C2H5OH、苛性钾、NaHSO4 |
| D、盐酸、SO2、纯碱、NH4Cl |