题目内容
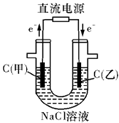
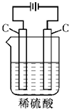
下列各装置中,烧杯中盛有海水,能够形成原电池并且铁为正极的是( )
A、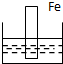 |
B、 |
C、 |
D、 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,能够形成原电池,说明符合原电池的构成条件,且铁作正极,则铁的活动性较负极材料弱.
解答:
解:A.该装置中没有两个电极,所以不能构成原电池,故A错误;
B.该装置中铁比Cu易失电子而作负极,故B错误;
C.该装置符合原电池构成条件,铁易失电子作负极、C作正极,故C错误;
D.该装置符合原电池构成条件,且锌易失电子作负极、铁作正极,故D正确.
故选D.
B.该装置中铁比Cu易失电子而作负极,故B错误;
C.该装置符合原电池构成条件,铁易失电子作负极、C作正极,故C错误;
D.该装置符合原电池构成条件,且锌易失电子作负极、铁作正极,故D正确.
故选D.
点评:本题考查了原电池原理,明确原电池的构成条件及金属失电子难易程度即可解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
能正确表示下列反应的离子方程式是( )
| A、Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
| B、用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+═Cu2++2H2O |
| C、硫酸亚铁溶液中加入酸化的双氧水:Fe2++2H++H2O2═Fe3++2H2O |
| D、用惰性电极电解熔融氯化钠:2Cl-+2H2O═Cl2↑+H2↑+2OH- |
下列物质按照混合物、非电解质、碱、酸式盐的顺序排列正确的是( )
| A、漂白粉、Cl2、氨水、NaHCO3 |
| B、福尔马林、苯、Cu2(OH)2CO3、明矾 |
| C、食醋、C2H5OH、苛性钾、NaHSO4 |
| D、盐酸、SO2、纯碱、NH4Cl |
下列操作或发生事故时的处理方法正确的是( )
| A、可用燃着的酒精灯引燃另一只酒精灯 |
| B、给试管里的液体加热时,试管应与桌面垂直 |
| C、凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
| D、浓硫酸不慎沾在皮肤上,应立即用干布擦掉,然后用水冲洗,最后再涂上3%~5%的小苏打溶液 |
某有机化合物6.2g在氧气中完全燃烧,只生成8.8g CO2和5.4g H2O.下列说法正确的是( )
| A、该化合物仅含碳、氢两种元素 |
| B、该化合物中碳、氢原子个数比为1:4 |
| C、无法确定该化合物是否含有氧元素 |
| D、该化合物中一定含有氧元素 |
下列离子方程式不正确的是( )
A、用铜电极电解NaCl溶液:2Cl-+2H2O
| ||||
| B、氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O | ||||
| C、漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO | ||||
| D、Cl2通入FeBr2溶液中,Cl2与FeBr2物质的量之比4:5:10Fe2++6Br-+8Cl2=10Fe3++3Br2+16Cl- |
NaNO2是一种食品添加剂,它能致癌.酸性KMnO4溶液与NaNO2的反应方程式是(未配平):MnO4-+NO2-+□→Mn2++NO3-+H2O.下列叙述中正确的是( )
| A、该反应中NO2-是还原剂 |
| B、反应过程中溶液的pH减小 |
| C、生成1mol NaNO3时消耗2.5mol KMnO4 |
| D、□中的粒子是OH- |