题目内容
10.下列条件下,两种气体的分子数一定相等的是( )| A. | 同质量不同密度的C2H4和CO | B. | 同温度同体积的C2H4和NO | ||
| C. | 同温度同压强的CO和N2 | D. | 同体积同压强的N2和N2H4 |
分析 A.CO和C2H4的摩尔质量相同,二者质量相同,则物质的量相同,分子数目之比等于物质的量之比;
B.同温度、同体积的C2H4和NO,影响二者物质的量的因素有压强,二者的压强不一定相同;
C.同温度同压强的CO和N2,具有相同的气体摩尔体积,而二者的体积不一定相等;
C.同压强、同体积的N2和N2H4,影响二者物质的量的因素有温度,二者的温度不一定相同.
解答 解:A.CO和C2H4的摩尔质量相同,二者质量相同,根据n=$\frac{m}{M}$可知,二者的物质的量相同,则二者含有分子数目相等,故A正确;
B.同温度、同体积的C2H4和NO,影响二者物质的量的因素有压强,二者的压强若相等,含有相同的分子数目,但二者压强不一定相同,含有分子数目不一定相等,故B错误;
C.同温度同压强的CO和N2,二者的气体摩尔体积相同,则二者的分子数取决于气体体积,没有告诉体积是否相等,则二者的分子数不一定相等,故C错误;
D.N2和N2H4,影响二者物质的量的因素有温度,二者的温度若相等,含有相同的分子数目,但二者温度不一定相同,所以含有分子数目不一定相等,故D错误;
故选A.
点评 本题考查了阿伏伽德罗定律及其推论,题目难度中等,明确各个物理量之间的关系是解本题关键,知道只有物质的量相等时其分子数才能相等,只要判断气体的物质的量是否相等即可.

练习册系列答案
相关题目
20.(1)短周期元素中原子核外p轨道上电子数与s轨道上电子总数相等的元素是O、Mg(写元素符号).
(2)Ti(BH4)2是一种重要的储氢材料.在基态Ti2+中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
(3)H2S和H2O2的主要物理性质如表所示:
H2S和H2O2的相对分子质量基本相同,造成上述物理性质差异的主要原因是H2O2分子之间会形成氢键,熔沸点高,H2O2与水分子之间会形成氢键,溶解度大.
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,与Ni(CO)n中配体互为等电子体的离子的化学式为CN-或C22-(写出一个即可).
(5)已知CrO5中Cr为+6价,则CrO5的结构式为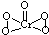 .
.
(2)Ti(BH4)2是一种重要的储氢材料.在基态Ti2+中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
(3)H2S和H2O2的主要物理性质如表所示:
| 熔点/K | 沸点/K | 水中的溶解度(标准状况) | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,与Ni(CO)n中配体互为等电子体的离子的化学式为CN-或C22-(写出一个即可).
(5)已知CrO5中Cr为+6价,则CrO5的结构式为
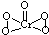 .
.
5.Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+Mg═Mg2++2Ag+2Cl-.有关该电池的说法不正确的是( )
| A. | Mg为电池的负极 | B. | 正极反应为:AgCl+e-═Ag+Cl- | ||
| C. | 不能被KCl 溶液激活 | D. | 可用于海上应急照明供电 |
15.在①丙烯②氯乙烯③苯④甲苯四种有机化合物中,分子内所有原子均在同一平面的是( )
| A. | ②③ | B. | ②④ | C. | ①③ | D. | ③④ |
2.下列除去括号内杂质的有关操作方法不正确的是( )
| A. | 乙烷(乙炔):通过盛溴水的洗气瓶 | |
| B. | 乙酸乙酯(乙醇):加入乙酸和浓硫酸的混合液,然后加热 | |
| C. | 苯(苯酚):加入氢氧化钠溶液,然后分液 | |
| D. | 乙醇(水):加入生石灰,然后蒸馏 |
20.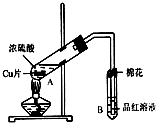 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
(1)写出试管B中的实验现象品红溶液褪色.
(2)写出A中反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O
(3)B试管口的棉花应沾有的试剂是NaOH.
(4)反应后有铜剩余,若不补充浓硫酸,要使铜片溶解,继续向A试管中加入H2O2,发现铜片又溶解,反应的离子方程式为:Cu+H2O2+2H+=Cu2++2H2O.或者可以加Fe2O3、NaNO3(填写两种属于不同类别物质的化学式),也能使铜片溶解.
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4•xH2O).小组成员采用加热法测定该晶体里结晶水x的值.
下面是其中一次实验的数据:
根据上表数据计算判断x的实侧值比理论值(x=5)偏小(填“偏大”、“偏小”),这次实验中产生误差的原因可能是AD(填序号)
A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却.
 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.(1)写出试管B中的实验现象品红溶液褪色.
(2)写出A中反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O
(3)B试管口的棉花应沾有的试剂是NaOH.
(4)反应后有铜剩余,若不补充浓硫酸,要使铜片溶解,继续向A试管中加入H2O2,发现铜片又溶解,反应的离子方程式为:Cu+H2O2+2H+=Cu2++2H2O.或者可以加Fe2O3、NaNO3(填写两种属于不同类别物质的化学式),也能使铜片溶解.
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4•xH2O).小组成员采用加热法测定该晶体里结晶水x的值.
下面是其中一次实验的数据:
| 坩埚质量 | 坩埚与晶体的总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.9g |
A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却.