题目内容
13.现有①铁片 ②饱和食盐水 ③液态氯化氢 ④乙醇 ⑤干冰 ⑥熔融KNO3 ⑦BaSO4固体⑧石墨 ⑨苛性钠,其中属于电解质的是③⑥⑦⑨(填序号,下同),属于非电解质的是④⑤,能导电的是①②⑥⑧.分析 根据电解质的定义分析,在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、活泼金属氧化物和水;非电解质是在水溶液里和熔融状态下都不能导电的化合物,包括一些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等);根据物质导电的原因分析,只要含有自由移动的离子或自由电子即可.
解答 解:①铁片是金属单质,有自由移动的电子,能够导电;既不是电解质也不是非电解质;
②饱和食盐水是混合物既不是电解质也不是非电解质,有自由移动的离子能导电;
③液态氯化氢只存在氯化氢分子不能导电,其水溶液能电离出氢离子和氯离子导电,为电解质;
④乙醇是化合物,但其水溶液只存在乙醇分子,不导电,属于非电解质;
⑤CO2只存在分子,没有自由移动的离子,所以不能导电;二氧化碳在水溶液中与水反应生成碳酸,碳酸电离出自由移动的离子导电,二氧化碳自身不能电离,二氧化碳是非电解质;
⑥熔融KNO3电离出自由移动的钾离子和硝酸根离子,能导电;它是化合物,属于电解质;
⑦BaSO4没有自由移动的离子不导电; 虽然硫酸钡在水中的溶解度很小,但硫酸钡只要溶解就完全电离且在熔融状态下能够完全电离,所以硫酸钡是电解质;
⑧石墨是单质既不是电解质也不是非电解质;有自由移动的电子,能够导电;
⑨苛性钠能电离出钠离子和氢氧根离子是电解质,但不能导电;电解质包括酸、碱、盐、活泼金属氧化物和水,所以③⑥⑦⑨符合;非电解质包括一些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等),所以④⑤是非电解质;能导电的是①②⑥⑧;
故答案为:③⑥⑦⑨;④⑤;①②⑥⑧.
点评 本题考查了电解质、非电解质的判断,根据物质的结构特点结合定义来分析即可,应注意的是电解质不一定导电,导电的不一定是电解质.

练习册系列答案
相关题目
1.下列有关实验原理或操作正确的是( )
| A. | 用湿润的pH试纸来测溶液的pH | |
| B. | 用四氯化碳萃取溴的苯溶液中的溴 | |
| C. | 实验室将硫酸铜溶液直接加热蒸干来制取CuSO4•5H2O | |
| D. | 用KSCN溶液检验硫酸亚铁溶液是否氧化变质 |
18.下列离子方程式不正确的是( )
| A. | 足量的溴化亚铁和少量的氯气反应:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 向KI与稀硫酸的混合溶液中通入氧气:4H++O2+4I-═2I2+2H2O | |
| C. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| D. | 碳酸氢镁溶液中加入足量的澄清石灰水:Mg2++2HCO3-+2Ca2++4OH-═Mg(OH)2↓+2CaCO3↓+2H2O |
5.下列离子方程式书写正确的是( )
| A. | 用Pt电极电解少量的MgC12溶液:2H2O+2Cl- $\frac{\underline{\;通电\;}}{\;}$H2↑+C12↑+2OH- | |
| B. | 明矾溶液中加入Ba(OH)2溶液至生成的沉淀的质量最多:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O | |
| C. | 向含有4 mol FeBr2的溶液中通入3 mol Cl2充分反应:2Fe2++4Br-+3Cl2═4Fe3++6Cl-+Br2 | |
| D. | 碳酸钙溶于醋酸中:CaCO3+2H+═Ca2++CO2↑+H2O |
2.下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A. | Cu(OH)2与盐酸,Cu(OH)2与醋酸 | |
| B. | BaCl2溶液与Na2SO4溶液,Ba(OH)2溶液与H2SO4溶液 | |
| C. | NaHCO3溶液与NaHSO4溶液,NaHCO3溶液与盐酸 | |
| D. | 石灰石与稀硝酸反应,生石灰与稀盐酸 |
 二氧化氯(ClO2)气体是一种常用高效的自来水消毒剂.
二氧化氯(ClO2)气体是一种常用高效的自来水消毒剂. .
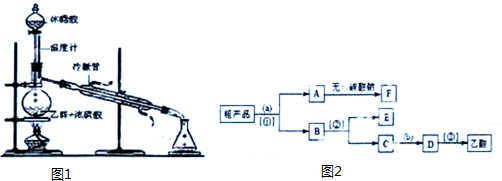
.
 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;