题目内容
4.下列说法中不正确的是( )| A. | 化学反应中的能量变化通常表现为热量的变化 | |
| B. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| C. | 吸热反应需要加热后才能发生 | |
| D. | 反应物总能量和生成物总能量的相对大小决定了反应是放出还是吸收能量 |
分析 A.化学反应中实质是化学键的断裂和形成;
B.根据化学反应中实质是化学键的断裂和形成;
C.根据反应是吸热反应还是放热反应与反应的条件无关;
D.△H=生成物的能量和-反应物的能量和.
解答 解:A.化学反应中实质是化学键的断裂和形成,断键吸收能量,成键放出能量,故A正确;
B.因化学反应中能量变化的主要原因是化学键的断裂和形成,故B正确;
C.因反应是吸热反应还是放热反应与反应的条件无关,如氯化铵与氢氧化钡晶体反应是吸热反应,却能自发发生,故C错误;
D.反应是放出还是吸收能量取决于反应物总能量和生成物总能量的相对大小,故D正确;
故选C.
点评 本题主要考查了化学反应中能量变化的原因,需要强调的是反应是吸热反应还是放热反应与反应的条件无关,难度不大.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
7.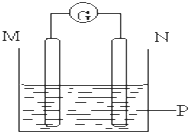 如图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的组合是( )
如图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的组合是( )
 如图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的组合是( )
如图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的组合是( )| M | N | P | |
| A | 锌 | 铜 | 稀硫酸溶液 |
| B | 铜 | 铁 | 稀盐酸溶液 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 锌 | 铁 | 硝酸铁溶液 |
| A. | A | B. | B | C. | C | D. | D |
8.下列实验方案可行的是( )
| A. | 用向下排空气法收集CO2 | B. | 用碱石灰干燥SO2 | ||
| C. | 通入Cl2出去FeCl3中FeCl2 | D. | 用HCl除去Na2CO3中的NaHCO3 |
12.下列反应的离子方程式正确的是( )
| A. | Na[Al(OH)4]溶液中通入过量CO2:2[Al(OH)4]-+CO2+3H2O=2Al(OH)3↓+CO32- | |
| B. | 往碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 氧化铜溶于稀盐酸中:CuO+2H+=Cu2++2H2O | |
| D. | 向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
19.下列各组物质不互为等电子体的是( )
| A. | CO和N2 | B. | CO2和N2O | C. | CO32-和NO3- | D. | CO2和SO2 |
9.对于化学反应3W(g)+2X(g)═4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
| A. | v(X)=v(Y) | B. | 3v(W)=2v(X) | C. | 2v(X)=v(Y) | D. | 2v(X)=3v(Z) |
16.概括中学化学有关知识,有气味的气体一般( )
| A. | 密度比空气大 | B. | 能溶于水 | ||
| C. | 有一定颜色 | D. | 沸点比其他气体低 |
14.下列各组离子,在强碱性溶液中可以大量共存的是( )
| A. | K+HCO3-NO3-ClO- | B. | Na+SO32-NH4+Ba2+ | ||
| C. | Ba2+ HS-Cl-SO42- | D. | AlO2-CO32-Cl-Na+ |