题目内容
19.下列各组物质不互为等电子体的是( )| A. | CO和N2 | B. | CO2和N2O | C. | CO32-和NO3- | D. | CO2和SO2 |
分析 原子数相同、价电子总数相同的粒子互称为等电子体.粒子中质子数等于原子的质子数之和,中性微粒中质子数=电子数,阳离子的电子数=质子数-电荷数,阴离子的电子数=质子数+电荷数.
解答 解:A、CO和N2的原子总数为2,价电子总数分别为4+6=10和5×2=10,两者均相同,故A不选;
B、CO2和N2O原子总数为3,价电子总数分别为4+2×6=16和2×5+6=16,二者分子中原子个数相等、价电子数相等,所以是等电子体,故B不选;
C、CO32-和NO3-原子总数为4,价电子总数分别4+3×6+2=24和5+3×6+1=24,两者均相同,故C不选;
D、CO2和SO2原子总数为3,价电子总数分别为4+2×6=16和6+2×6=18,价电子数不同,不是等电子体,故D选.
故选:D.
点评 本题主要考查等电子体、学生对信息的理解与直接运用,比较基础,注意基础知识的掌握.

练习册系列答案
相关题目
14.短周期元素R、Q、M、T在元素周期表中的相对位置如表,已知R原子最外层电子数与次外层电子数之比为2:1.
(1)人的汗液中含有T的简单离子,其离子结构示意图为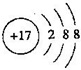 ; 元素M在元素周期表中的位置是第三周期第VIA族.
; 元素M在元素周期表中的位置是第三周期第VIA族.
(2)R的最高价氧化物所含的化学键类型是共价键(选填“离子”或“共价”).
(3)加热时,Q的最高价氧化物对应水化物的浓溶液与单质R反应的化学方程式为4HNO3(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+CO2↑+2H2O(用具体的化学式表示).
(4)在一定条件下甲、乙、丙有如下转化:甲$\stackrel{+X}{→}$乙$→_{化合反应}^{+X}$丙,若其中甲是单质,乙、丙为化合物,x是具有氧化性的无色气体单质,则甲的化学组成不可能是④(选填序号).
①R ②Q2 ③M ④T2
(5)元素T的含氧酸HTO具有漂白性写出HTO的电子式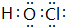 .
.
| R | Q | ||
| M | T |
 ; 元素M在元素周期表中的位置是第三周期第VIA族.
; 元素M在元素周期表中的位置是第三周期第VIA族.(2)R的最高价氧化物所含的化学键类型是共价键(选填“离子”或“共价”).
(3)加热时,Q的最高价氧化物对应水化物的浓溶液与单质R反应的化学方程式为4HNO3(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+CO2↑+2H2O(用具体的化学式表示).
(4)在一定条件下甲、乙、丙有如下转化:甲$\stackrel{+X}{→}$乙$→_{化合反应}^{+X}$丙,若其中甲是单质,乙、丙为化合物,x是具有氧化性的无色气体单质,则甲的化学组成不可能是④(选填序号).
①R ②Q2 ③M ④T2
(5)元素T的含氧酸HTO具有漂白性写出HTO的电子式
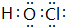 .
.
4.下列说法中不正确的是( )
| A. | 化学反应中的能量变化通常表现为热量的变化 | |
| B. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| C. | 吸热反应需要加热后才能发生 | |
| D. | 反应物总能量和生成物总能量的相对大小决定了反应是放出还是吸收能量 |
11.在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时B的浓度是原来的35%,则( )
| A. | 物质A的转化率大了 | B. | a<b | ||
| C. | 物质B的质量分数减小了 | D. | 平衡向正反应方向移动了 |
8.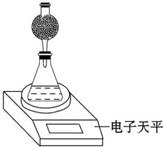 某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.限选试剂:1.00mol•L-1 HNO3、2.00mol•L-1 HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴.
某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.限选试剂:1.00mol•L-1 HNO3、2.00mol•L-1 HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴.
(1)他们能完成哪些因素对速率影响的探究?
探究同体积下HNO3浓度对该反应剧烈程度的影响、探究接触面积对该反应剧烈程度的影响、探究温度对该反应剧烈程度的影响.
(2)请根据能进行的探究内容,填写以下实验设计表,完成探究实验:
(3)整个实验中应控制的不变量是硝酸溶液体积和CaCO3质量.
(4)该实验小组用如图实验装置进行实验.
①除电子天平、干燥管、锥形瓶、药匙、胶塞等仪器外,必需的实验仪器还有量筒、秒表.
②干燥管中应放置的试剂是BC.
A.碱石灰 B.无水CaCl2C.P2O5固体 D.浓硫酸
③若撤除干燥管装置,所测速率偏大(填“偏大”、“偏小”或“不变”).
 某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.限选试剂:1.00mol•L-1 HNO3、2.00mol•L-1 HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴.
某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.限选试剂:1.00mol•L-1 HNO3、2.00mol•L-1 HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴.(1)他们能完成哪些因素对速率影响的探究?
探究同体积下HNO3浓度对该反应剧烈程度的影响、探究接触面积对该反应剧烈程度的影响、探究温度对该反应剧烈程度的影响.
(2)请根据能进行的探究内容,填写以下实验设计表,完成探究实验:
| 实验编号 | T/℃ | 大理石规格 | HNO3浓度/mol•L-1 |
| ① | 常温 | 2.00 | |
| ② | 1.00 | ||
| ③ | 2.00 | ||
| ④ | 2.00 |
(4)该实验小组用如图实验装置进行实验.
①除电子天平、干燥管、锥形瓶、药匙、胶塞等仪器外,必需的实验仪器还有量筒、秒表.
②干燥管中应放置的试剂是BC.
A.碱石灰 B.无水CaCl2C.P2O5固体 D.浓硫酸
③若撤除干燥管装置,所测速率偏大(填“偏大”、“偏小”或“不变”).
9.乙醇分子中的各种化学键如图所示,下列关于乙醇在各种反应中断裂键的说明不正确的是( )
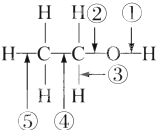

| A. | 和金属钠反应时①键断裂 | |
| B. | 在铜催化及加热条件下与O2反应时断裂①键和③键 | |
| C. | 在铜催化及加热条件下与O2反应时断裂①键和⑤键 | |
| D. | 在空气中完全燃烧时断裂①②③④⑤键 |
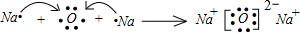
 或
或

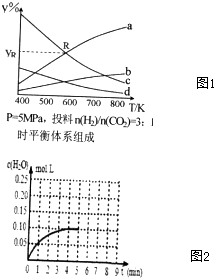 环境问题正引起全社会关注,CO、CO2的应用对构建生态文明有重要意义.
环境问题正引起全社会关注,CO、CO2的应用对构建生态文明有重要意义.